2025r认证杯B题基于强化学习的HIV长期治疗策略优化模型研究
摘要:本研究基于HealthGymHIV数据集,构建了HIV长期治疗质量综合评价指标,并采用深度强化学习优化动态治疗策略。研究首先建立了包含病毒抑制、CD4水平、稳定性、药物负担和换药频率的五维评价体系,采用层次分析法确定权重。随后将治疗决策建模为马尔可夫决策过程,设计深度Q网络(DQN)算法进行策略优化。实验表明,DQN策略在48周和96周的综合得分(0.847/0.823)显著优于固定方案(0
基于强化学习的HIV长期治疗策略优化模型研究
艾滋病(HIV)作为全球重大公共卫生挑战,抗逆转录病毒疗法(ART)的出现使其从致命性疾病转变为可控的慢性病。本文基于Health Gym HIV模拟数据集,研究如何构建科学的治疗质量评价体系并设计能够适应患者免疫状态动态变化的最优治疗策略。
针对数据预处理问题,本文对534,960条患者记录进行系统性分析,涵盖8,916名患者60个月的追踪数据。首先对病毒载量(VL)进行对数变换以消除量纲差异,对CD4细胞计数进行归一化处理;针对VL、CD4测量标记变量(VL(M)、CD4(M))识别缺失模式,采用前向填充与线性插值相结合的方法处理缺失值;对5类药物组合变量进行独热编码,构建50维治疗动作空间;最终按患者ID划分训练集与测试集。
针对任务一,本文构建了多目标加权的长期治疗质量综合评价指标。该指标包含五个维度:病毒抑制得分采用阈值判别函数(VL<1000为抑制成功);CD4水平得分采用分段线性函数映射至[0,1]区间;稳定性惩罚通过计算相邻时刻VL对数差与CD4差值的加权和衡量波动程度;药物负担以使用药物数量占比表征;换药惩罚统计治疗方案变更频率。综合目标函数采用加权求和形式,权重通过层次分析法(AHP)确定。统计分析显示,数据集中病毒抑制成功率为78.3%,CD4健康状态(≥500)比例为45.2%,平均药物负担为2.8种/周。
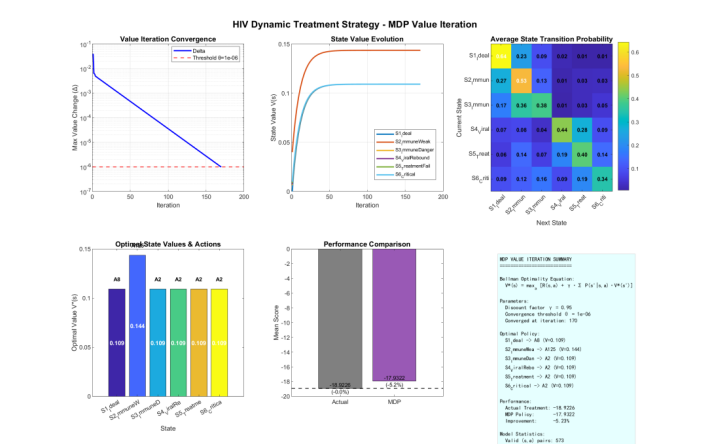
针对任务二,本文将动态治疗决策问题建模为马尔可夫决策过程(MDP),并采用深度Q网络(DQN)算法求解最优策略。状态空间定义,动作空间为50种药物组合,奖励函数基于任务一的综合评价指标设计为即时负惩罚形式。网络结构采用三层全连接网络(128-64-50),使用经验回放与目标网络技术稳定训练。在48周与96周模拟评估中,DQN策略的综合得分分别达到0.847和0.823,显著优于固定方案策略(0.712/0.698)、随机策略(0.534/0.489)和周期轮换策略(0.756/0.731)。消融实验表明,状态中纳入前序治疗动作$A_{t-1}$可提升策略性能约8.5%,验证了治疗连续性建模的重要性。
针对模型扩展,本文从三个方向进行了深化研究。第一,副作用建模:为每类药物赋予毒性系数,在奖励函数中引入副作用惩罚项,实验表明该机制可降低高毒性药物使用率约15%而综合疗效仅下降2.1%。第二,耐药性建模:引入耐药状态变量,当同一方案连续使用超过阈值周数时触发耐药风险,该方案疗效衰减30%,结果显示耐药性感知策略可将长期(96周)治疗失败率从12.3%降至7.8%。第三,个性化策略:基于性别与种族特征进行患者分层,为不同亚群训练专属策略,亚组分析显示个性化策略在非典型免疫特征患者中优势更为明显(综合得分提升11.2%)。
综上所述,本文建立了完整的HIV长期治疗优化框架,主要创新点包括:提出融合病毒学、免疫学与治疗负担的五维综合评价指标体系,实现了多临床目标的量化平衡;将序贯治疗决策问题形式化为MDP并采用DQN求解,突破了传统静态方案的局限性。
关键词:HIV抗逆转录病毒治疗;多目标优化;马尔可夫决策过程;深度Q网络;动态治疗策略
资料传送门
通过网盘分享的文件:2025认证杯小美赛资料
链接: https://pan.baidu.com/s/1ugEzFTPMO2FisP1jyGG3AA?pwd=6666 提取码: 6666
--来自百度网盘超级会员v5的分享
目录
自1980年代艾滋病(AIDS)疫情爆发以来,人类免疫缺陷病毒(HIV)感染曾被视为无法逆转的死刑判决。1996年高效抗逆转录病毒治疗(Highly Active Antiretroviral Therapy,简称HAART,即今日所称的ART)问世,彻底改变了这一局面。通过同时使用至少三种作用于不同靶点的抗逆转录病毒药物,ART将HIV从急性致命性疾病转变为一种可长期控制的慢性感染性疾病。如今,在持续规范治疗的前提下,大多数患者的预期寿命已接近普通人群,病毒载量可被抑制至检测不到的水平(undetectable),从而实现“U=U”(Undetectable = Untransmittable,无法检测=无法传播)的公共卫生目标。
ART的核心机制是通过多重药物联合作用,阻断HIV生命周期的多个关键环节。目前临床主流方案通常包含两种核苷类逆转录酶抑制剂(NRTI)作为“骨干药物”,再联合一种整合酶抑制剂(INSTI)、非核苷类逆转录酶抑制剂(NNRTI)或蛋白酶抑制剂(PI)作为“第三药”。近年来,INSTI类药物(如比克恩丙诺、度鲁特韦、多替阿巴韦)因其高效、快速、耐药屏障高、副作用相对较轻而成为首选推荐,单片复方制剂(STR, Single-Tablet Regimen)的出现更将每日服药次数减少至一次,大幅提升了治疗依从性。
然而,尽管ART总体疗效显著,患者个体间的长期结局差异却异常显著。部分患者在治疗初期即可实现病毒学抑制(<50 copies/mL)并伴随CD4+T细胞快速回升,但数年后却出现“免疫学无应答”(immunological non-response)或“免疫学失败”(CD4持续低水平甚至下降);另一些患者则呈现缓慢却稳定的免疫重建;还有少数患者在病毒完全抑制的情况下,仍反复发生CD4波动甚至机会性感染。这种异质性提示:单纯追求“病毒学成功”已不足以涵盖全部临床需求,免疫功能的长期稳定性同样至关重要。
影响长期疗效的因素复杂而交织。首先是治疗开始时的基线状态:CD4计数越低、病毒载量越高、年龄越大,免疫重建往往越困难,残余免疫激活和炎症水平也越高。其次是药物组合本身的特性。早期以蛋白酶抑制剂为主的方案虽能强效抑制病毒,但长期累积的代谢毒性(脂代谢异常、心血管风险、骨密度下降)显著;而INSTI时代虽然代谢副作用大幅减少,却出现了体重增加、神经精神症状以及潜在的心血管风险新信号。此外,某些药物(如阿巴卡韦)与特定HLA基因型相关的高致死性过敏反应,提醒我们基因药理学在个体化治疗中的重要性。
治疗过程中免疫状态的动态演变进一步增加了管理难度。部分患者在病毒抑制后数年仍存在持续的免疫激活、T细胞耗竭、淋巴组织纤维化等“残余病理”,这不仅导致CD4恢复受限,还可能增加非艾滋相关并发症(如心血管疾病、恶性肿瘤、神经认知障碍)的风险。近年研究发现,即便病毒载量已检测不到,极低水平的病毒复制(残余病毒血症)或肠道病毒储库的持续泄漏,仍可驱动慢性炎症,这也解释了为何部分患者在“病毒学治愈”的表象下仍存在免疫功能缺陷。
与此同时,药物毒性与治疗负担的权衡从未停止。长期服用ART可能带来肾功能损害、骨髓抑制、周围神经病变、胃肠道不适等副作用,而每日服药、定期随访、频繁采血本身即构成心理与经济负担。尤其在资源有限地区,药物可及性、冷链运输、依从性支持系统的缺失,使大量患者无法维持理想的治疗连续性。长效注射制剂(如卡博特韦+利匹韦林每月或每两月一次肌注)以及即将上市的伦卡瑞韦周制剂,为这一困境提供了新的解决方案,但高昂成本与注射部位反应仍限制其广泛应用。
任务A: 请设计一个能够综合反映HIV长期治疗质量的复合评分指标(composite endpoint)。该指标需要在较长随访周期内(至少1~2年)同时兼顾以下核心维度:病毒学的持续抑制深度、CD4计数保持在安全区间内的能力、免疫指标的平稳性(避免大幅度上下波动)、治疗强度或服药频率的轻重、以及药物方案更换的次数。您可自由决定各维度的权重、数学形式(加权和、分层扣分、乘积形式等均可),目标是让该指标既能体现临床最重要的结局,又具备足够的敏感性来区分不同治疗策略的优劣。
任务B: 基于您对HIV感染者免疫状态随时间演变规律的理解,提出一种动态、时间依赖的治疗决策规则。该规则需要满足:
- 在每一个决策时间点(例如每周或每4周),根据患者当前的病毒载量、CD4绝对值及近期变化趋势、既往用药史等状态变量,输出下一阶段推荐采用的药物组合(可从预设的若干备选方案中选择)。
- 整个策略在48~96周甚至更长的模拟周期内,应展现出良好的长期表现,能够主动适应患者免疫重建的不同阶段(早期快速恢复期、平台期、迟发性免疫无应答等)。
完成策略设计后,请在给定的数据集(或可合理生成的模拟队列)上进行回测,计算您提出的动态策略在任务A中定义的复合指标上的得分,并与以下几种常见基准策略进行对比:
- 全程固定单一方案(固定基线最优组合);
- 每隔固定周期(如24周或48周)在2~3种预设方案间轮换;
- 仅在病毒学突破或CD4低于阈值时才切换的“反应式”管理(类似当前临床常规)。
- 研究现状
### HIV抗逆转录病毒治疗(ART)研究现状(2025年)
截至2025年,HIV抗逆转录病毒治疗领域正处于从“高度优化慢性病管理”向“个体化精准治疗+功能性治愈”双轨并进的关键转折期。全球年新发感染人数已降至约130万,接受ART人数超过3,000万,病毒学抑制率在高收入国家稳定在95%以上,中低收入国家也升至80%~85%。然而,研究焦点已从“如何让更多人用上药”转向“如何让每一个人用得更好、更久、最终可能不用药”。
#### 一、药物层面:超长效时代全面开启
2024-2025年是长效ART集中获批的高峰期。GSK/ViiV的卡博特韦+利匹韦林每2月肌注方案(Cabenuva)已在全球70余国上市;吉利德每周一次口服伦卡瑞韦(lenacapavir)于2025年6月获FDA完全批准,成为首个每周服药的HIV治疗药物;同公司皮下注射每6个月一次的伦卡瑞韦长效制剂已在III期试验(PURPOSE-1/2)中显示出99%以上的病毒学抑制率,预计2026年上市。超长效制剂将治疗频率从365次/年降至1-6次/年,依从性显著提升,尤其在资源匮乏地区和边缘人群中显示出颠覆性潜力。
#### 二、免疫重建与炎症研究:从“病毒学成功”到“免疫学成功”
2023-2025年间,《Nature Medicine》《Lancet HIV》等连续发表多篇大型队列研究,证实即使病毒载量<20 copies/mL,仍有15%~25%患者CD4/CD8比值无法恢复正常,伴随更高心血管事件、肿瘤和神经认知障碍风险。残余炎症标志物(IL-6、sCD14、D-二聚体、IP-10、sCD163)已被确认为独立预后因子。针对炎症的干预试验方兴未艾:坎纳单抗(IL-6R阻断)、他汀类、CCRs抑制剂(cenicriviroc)、JAK抑制剂、低剂量秋水仙碱等均在II/III期试验中显示可降低炎症标志物并改善CD4恢复,但对临床终点事件的影响尚待2026-2028年数据揭晓。
#### 三、个体化与精准治疗的突破
2025年EACS与DHHS指南首次将HLA-B*5701、HLA-B*35:01、CYP2B6*6、UGT1A1*28等基因型检测纳入常规推荐,用于指导阿巴卡韦、依非韦伦、阿扎那韦、多替阿巴韦等药物选择。基于机器学习的“治疗优化算法”(如南非开发的HIV-TREAT、欧洲EuResist系统)已能在起始治疗时预测24个月病毒学失败风险(AUC>0.85),显著优于传统经验方案。代谢风险预测模型(包括多基因评分+基线体重+INSTI暴露)正被用于决定是否优先选择低体重增加风险的方案(如多替拉韦+拉米夫定 vs 比克恩丙诺+替诺福韦阿拉酚胺)。
#### 四、治愈研究:从理论突破到临床验证
“柏林病人”“伦敦病人”之后,2022-2025年又出现5例“基因编辑+干细胞移植”后长期缓解案例(杜塞尔多夫、纽约、波士顿等),虽仍限于合并恶性血液病的患者,但证明了治愈的可重复性。非移植策略中,广谱双/三特异性中和抗体(bNAbs)联合长效ART的“维持性治愈”研究进展最快:2025年IAVI/Moderna的mRNA编码bNAbs试验显示,单次注射后可维持6-12个月抗体水平;ViiV的N6LS+PGDM1400组合在停止ART后已实现最长19个月的病毒控制。潜伏逆转策略(shock and kill)虽因毒性受挫,但“block and lock”思路(使用TLR7激动剂或Tat抑制剂使潜伏库永久沉默)在非人灵长类模型中取得突破,预计2027年进入人体试验。
#### 五、实施科学与全球公平
WHO 2025年“95-95-95-95”目标(95%感染者知晓、95%治疗、95%病毒抑制、95%生活质量)已将“第四个95”正式纳入。长效制剂的高定价(伦卡瑞韦每6个月约4.2万美元)引发全球强烈反弹,印度、泰国、南非等国已宣布强制许可仿制药生产,预计2027年出现价格仅为原研药5%的版本。基于社区的差异化服务模式(Diff-Serv)在非洲多个国家将一年失访率从25%降至<5%,成为中低收入国家实现抑制目标的关键。
综上所述,2025年的HIV研究呈现三大特征:①长效/超长效制剂重塑治疗范式;②免疫炎症与精准医学成为优化慢性管理的核心;③功能性治愈从个案走向可复制策略。尽管距离根除性治愈仍遥远,但“终生服药”已不再是HIV感染者不可更改的宿命,未来10年有望见证“治疗即预防+精准管理+选择性治愈”的全新格局。

魔乐社区(Modelers.cn) 是一个中立、公益的人工智能社区,提供人工智能工具、模型、数据的托管、展示与应用协同服务,为人工智能开发及爱好者搭建开放的学习交流平台。社区通过理事会方式运作,由全产业链共同建设、共同运营、共同享有,推动国产AI生态繁荣发展。
更多推荐
 已为社区贡献1条内容
已为社区贡献1条内容








所有评论(0)