Nature子刊|基于超声成像的可解释多模态深度学习预测甲状腺癌侧方淋巴结转移
这篇发表于《Nature Communications》的研究针对甲状腺癌侧方淋巴结转移(LLNM)术前预测的临床需求,提出了一种名为LLNM-Net的双向注意力深度学习模型。该模型融合了术前超声图像、放射报告、病理结果及人口统计学数据等多模态信息,训练数据涵盖7个中心的29,615名患者和9836例手术案例。
小罗碎碎念
这篇发表于《Nature Communications》的研究针对甲状腺癌侧方淋巴结转移(LLNM)术前预测的临床需求,提出了一种名为LLNM-Net的双向注意力深度学习模型。

该模型融合了术前超声图像、放射报告、病理结果及人口统计学数据等多模态信息,训练数据涵盖7个中心的29,615名患者和9836例手术案例。
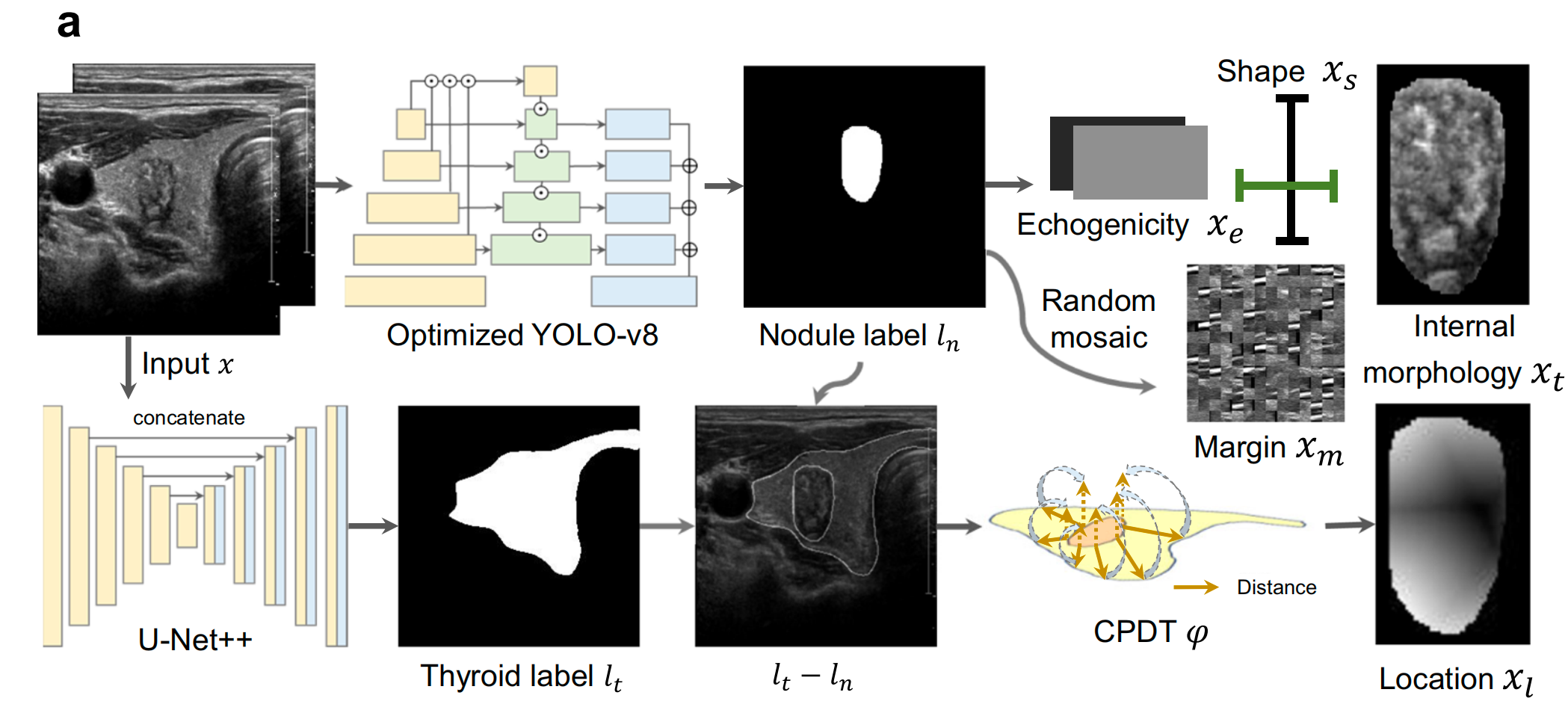
其核心架构包括前景优化分割、中心点距离变换(CPDT)等模块,通过甲状腺多模态深度学习(TMDL) transformer实现影像特征与临床文本的双向注意力交换,不仅在多中心测试中达到0.944的AUC和84.7%的准确率,显著优于人类专家(64.3%准确率)和现有模型,还能通过注意力热图和3D风险热图提供可解释的预测依据,例如识别出距甲状腺被膜0.25cm内的肿瘤转移风险超72%,以及中上叶为高风险区域。
在模型性能与临床价值方面,LLNM-Net展现出强大的泛化能力和风险分层能力,针对高风险患者识别的AUC可达0.983,且通过特征贡献分析明确了肿瘤位置(48.8%)、形态特征(29.9%)及临床文本信息(19.7%)在预测中的关键作用。
研究还通过与108名影像专家的对比实验,证实模型在LLNM预测上的准确性远超人类,同时其决策曲线分析显示,基于模型的策略能有效提升侧方淋巴结细针穿刺(FNA)的识别效率,减少不必要的侵入性操作。
此外,模型提供的定性和定量解释(如Sankey图展示特征贡献)提升了临床医生对AI结果的理解度,为术前筛查和手术策略制定提供了可靠工具。
从技术创新与应用前景来看,该研究解决了超声图像中前景小、背景差异大等挑战,通过CPDT方法精确提取肿瘤位置信息,并利用双向注意力机制有效融合多模态数据,其端到端的特征提取方法可推广至其他疾病的影像诊断任务。
![b 内部形态学注意力可视化。各列分别显示超声图像、对应特征图像及LLNM-Net中的注意力热图。热图中的热点区域代表模型关注重点,注意力分数越高表明该区域获得的模型关注度越大。图中所示结节均为恶性病例。在形态特征面板中,模型更关注结节的整体形态学特征,这表明结节内部纹理特征对模型预测淋巴结转移(LLNM)具有更显著贡献。色标标注为"注意力分数[AU]",数值范围从0.0(蓝色)至1.0(红色)。](https://i-blog.csdnimg.cn/img_convert/2fd928964264fbdb39a029a2663459fa.png)
目前,模型的3D风险热图已公开(https://snowinbio.github.io/LLNM-Net/),代码和部分数据集也可通过GitHub和Hugging Face获取,为后续研究提供了可复现的基础。
尽管存在病例类型和临床效益验证的局限,但该工作为医学AI在肿瘤转移预测领域的可解释性研究和临床转化提供了重要参考,尤其在优化诊疗流程、提高医疗资源分配效率方面具有显著潜力。
交流群
欢迎大家加入【医学AI】交流群,本群设立的初衷是提供交流平台,方便大家后续课题合作。
目前小罗全平台关注量71,000+,交流群总成员1600+,大部分来自国内外顶尖院校/医院,期待您的加入!!
由于近期入群推销人员较多,已开启入群验证,扫码添加我的联系方式,备注姓名-单位-科室/专业,即可邀您入群。
罗小罗团队
作者是一支以国内外硕博为主的学生团体,覆盖医学AI主流研究领域;团队现有50余人,持续欢迎新的小伙伴加入!
团队官网上传了大量优质的学习资料,包括但不限于每次免费公开课的回放,顶刊复现教程等等!
感兴趣的可以扫码或者点击链接访问作者团队的官网:https://www.lxltx.site/
一、引言
术前预测侧方淋巴结转移(LLNM)对于甲状腺癌的手术规划和预后管理至关重要。
LLNM结果呈阳性通常表明肿瘤已开始更广泛地扩散,促使医生采取更积极的治疗策略,这可能包括扩大手术范围并考虑术后放疗或化疗 14{}^{14}14 。
文献 15,16{}^{{15},{16}}15,16 表明,LLNM与较差的预后相关;与中央区淋巴结转移的患者相比,复发率显著更高 (60%({60}\%(60% 对比 30%,P=0.007){30}\% ,P = {0.007})30%,P=0.007) 。无病生存期和平均复发时间也明显更短(分别为30个月对52个月, P=0.035P = {0.035}P=0.035 ,以及7个月对44个月, P=0.004P = {0.004}P=0.004 ) )15{)}^{15})15 。
因此,有效预测LLNM可使医生制定更合适的治疗方案,降低因漏切导致癌症进展的风险,并更准确地评估患者预后,提供更全面的支持和护理 3,16{}^{3,{16}}3,16 。
在某些情况下,患者可能出现跳跃转移——中央区阴性而侧方区阳性 17,18{}^{{17},{18}}17,18 ——这在术前评估和手术中容易被遗漏 19{}^{19}19 。
此外,不同肿瘤类型的跳跃转移预后各不相同 20,21{}^{{20},{21}}20,21 ,这表明临床医生应考虑肿瘤的特定生物学特征和淋巴系统的解剖路径 13{}^{13}13 。
目前,术前淋巴结活检是评估LLNM的标准方法 3{}^{3}3 ;然而,超声引导下细针穿刺存在局限性,如穿刺不准确或漏穿 3,22{}^{3,{22}}3,22 。
鉴于LLNM的特殊重要性,迫切需要能够有效预测LLNM的术前评估方法,协助临床医生确定疾病性质并采取适当措施,从而为提高患者生存率做出重大贡献。
目前的研究表明,颈部淋巴结转移与原发肿瘤的组织形态和位置密切相关 6,23,24{}^{6,{23},{24}}6,23,24 。
具体而言,它通常是由原发肿瘤(甲状腺结节)的生长和扩散引起的,不同肿瘤类型表现出不同的转移倾向。
例如,异常增大的肿瘤可能是淋巴结转移的重要迹象 25{}^{25}25 ,而形态或质地异常的肿瘤也可能提示转移的可能性 6,26{}^{6,{26}}6,26 。
此外,原发肿瘤的生长位置会影响肿瘤细胞侵入淋巴系统的途径,增加上极转移的可能性 23,24{}^{{23},{24}}23,24 ,并影响不同区域淋巴结转移的风险和预后 3,15{}^{3,{15}}3,15 。
超声成像以其无创、实时和便捷的特点,成为甲状腺癌最常用的诊断方法之一。
它有助于医生检测早期肿瘤异常,如大小增加、形状不规则和内部结构异常,从而在侧方淋巴结转移(LLNM 27−29{}^{{27} - {29}}27−29 )中发挥预测作用。
然而,它存在器官间对比度低和图像质量差的问题,评估结果在很大程度上依赖于医生的经验。深度学习技术可以通过学习肿瘤形态、大小和钙化等图像特征来增强肿瘤识别 6,30−33{}^{6,{30} - {33}}6,30−33 。
前景-背景算法和图卷积网络等技术对位置信息进行统计分析 7{}^{7}7 ,协助医生进行术前诊断和预后评估,包括肿瘤恶性程度分级、亚型评估和颈部淋巴结转移预测 34,35{}^{{34},{35}}34,35 。
然而,目前缺乏大规模队列研究和用于精确分析LLNM的高效智能工具 16,27,36−38{}^{{16},{27},{36} - {38}}16,27,36−38 ,其结论往往缺乏定性/定量解释 23,24{}^{{23},{24}}23,24 。
在此,作者展示了LLNM-Net,这是一种双向注意力架构,用于整合多模态数据以进行术前LLNM预测。
如图1a所示,作者采用前景优化分割 39,40{}^{{39},{40}}39,40 和中心点距离变换(CPDT 41{}^{41}41 )来提取肿瘤形态和精确位置。
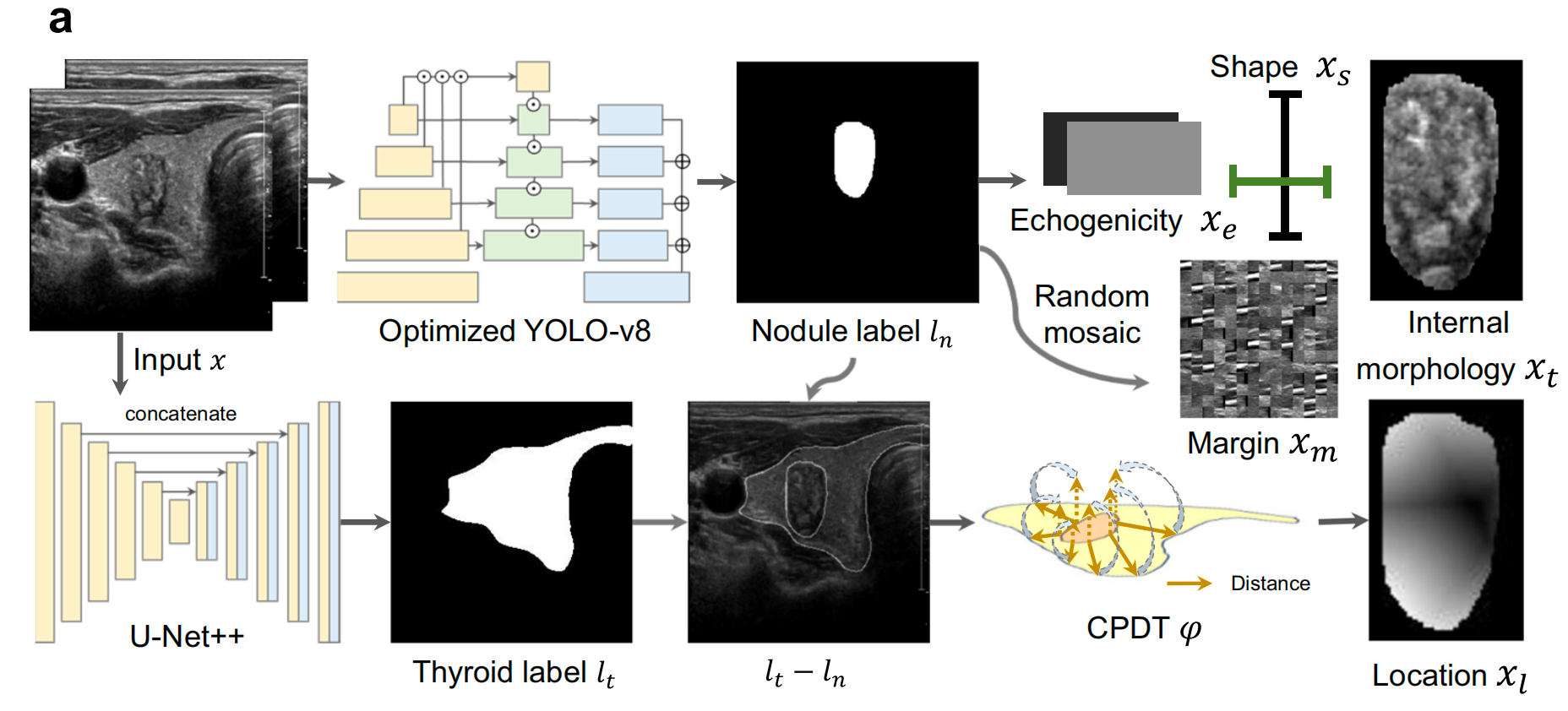
作者提出的甲状腺多模态深度学习(TMDL)变换器 42{}^{42}42 (图1b)通过双向注意力交换 43−45{}^{{43} - {45}}43−45 将成像特征与临床报告和人口统计学数据融合。
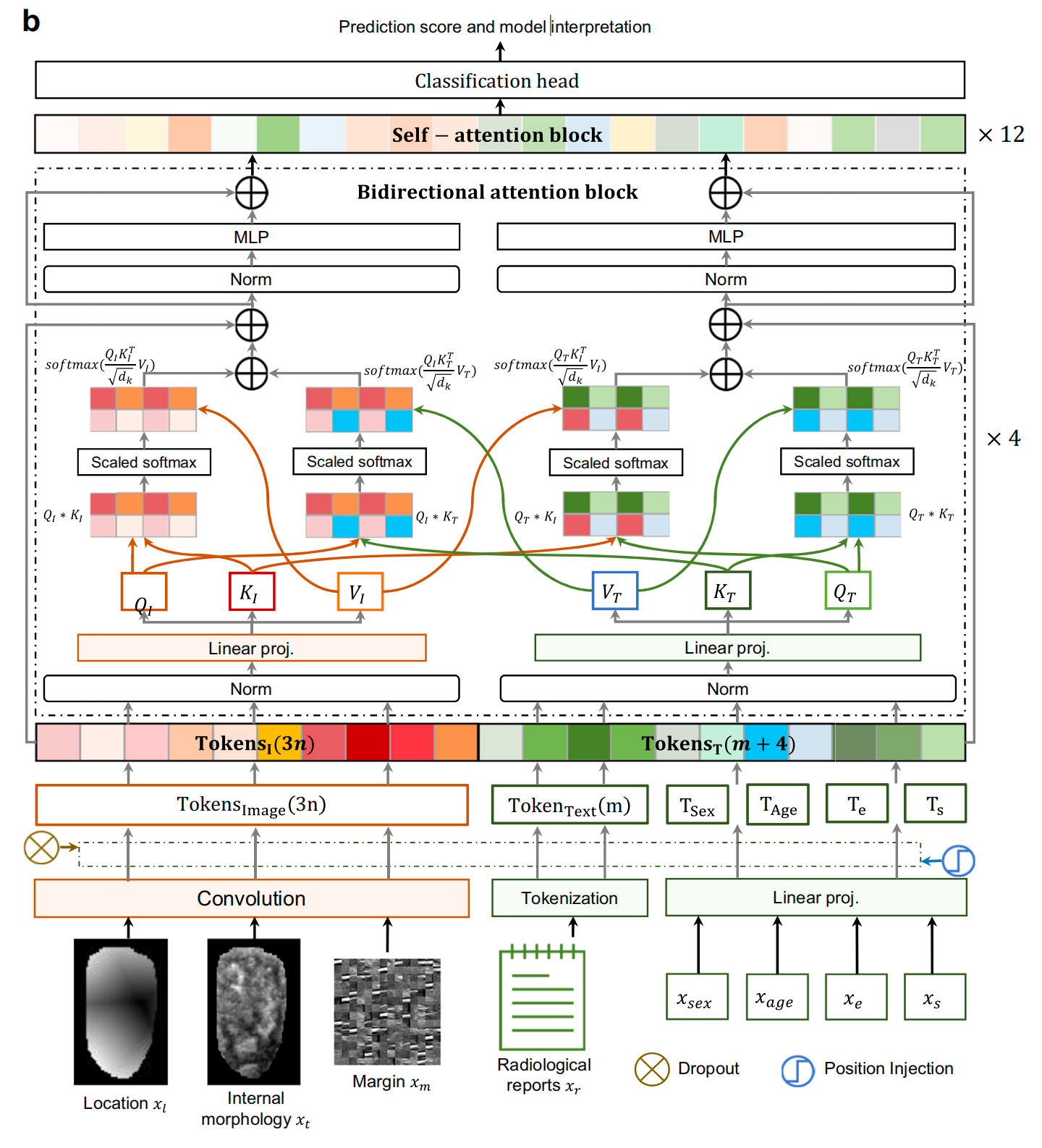
作者通过微分同胚配准生成3D风险热图,并进行基于注意力的梯度分析以解释转移机制。
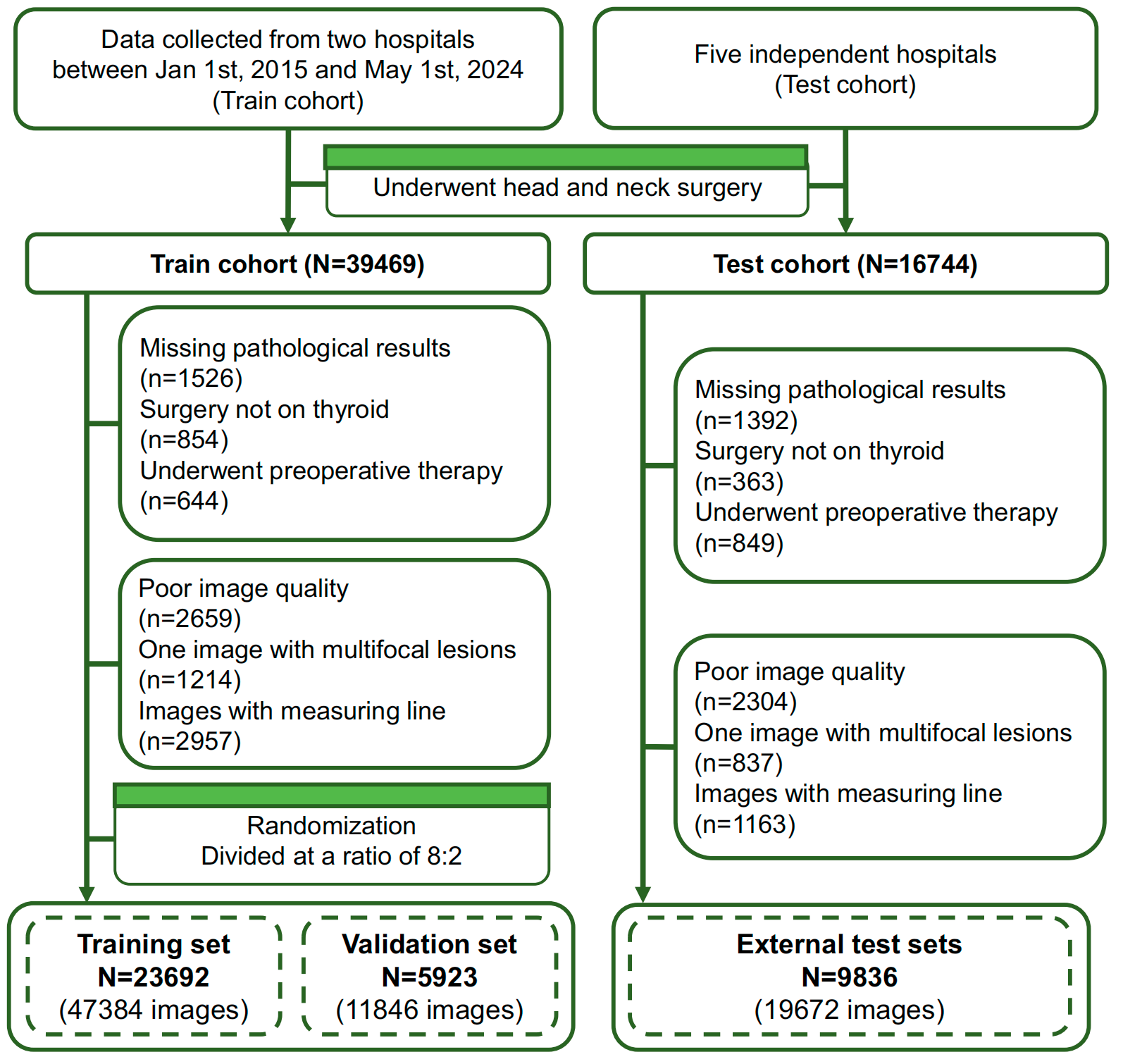
在来自七个机构的39451名患者(图2)上进行评估,LLNM-Net提供定量术前评估,以指导手术规划和预后管理。
二、结果
数据描述
作者收集了39451名患者的病理诊断、术前超声图像、放射学报告和人口统计学信息(表1)。
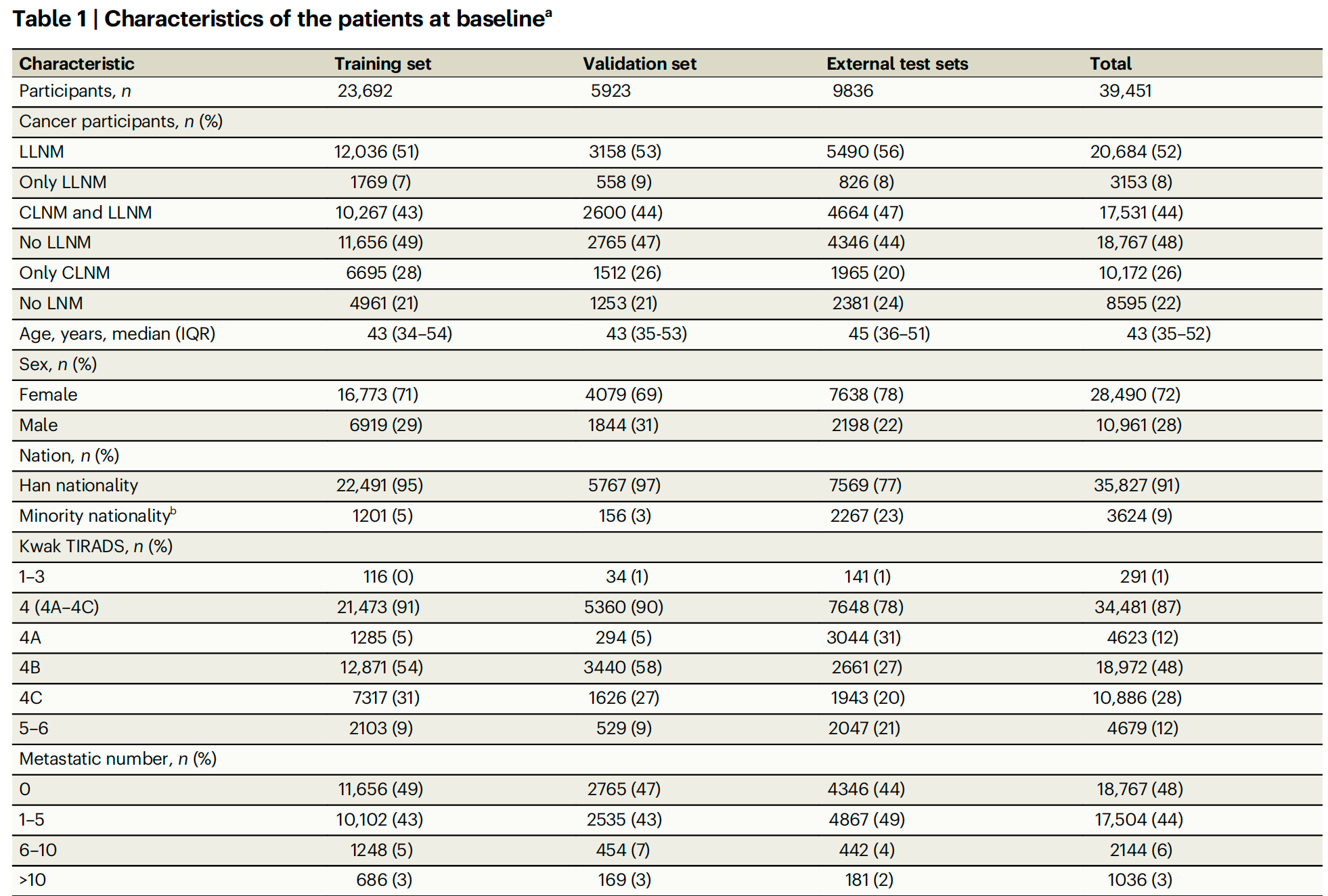
值得注意的是,年龄中位数为43岁,女性患者人数是男性患者的两倍多,并且该队列中约 91%{91}\%91% 为汉族。在Kwak甲状腺影像报告和数据系统(Kwak-TIRADS 46{}^{46}46 )中最常见的类别是4B(48%)和 4C(28%)4\mathrm{C}\left( {{28}\% }\right)4C(28%) 。
甲状腺结节小于 10 mm{10}\mathrm{\;{mm}}10mm 的患者占73%,LLNM阳性患者的比例为52%。收集的亚型包括35804例乳头状甲状腺癌(PTC)、2845例滤泡状甲状腺癌(FTC)和802例髓样甲状腺癌(MTC)。
作者使用来自两家医院的29615名患者中的80%训练模型,其余 20%{20}\%20% 用于模型验证。外部测试集包括来自五个多中心站点的9836名患者。更详细的信息可在表S1和S2中找到。
模型和人类专家的预测性能
图3a显示,LLNM-Net表现出显著优越的预测性能,在验证集上的曲线下面积(AUC)为0.948(95%置信区间:0.946 - 0.950)。
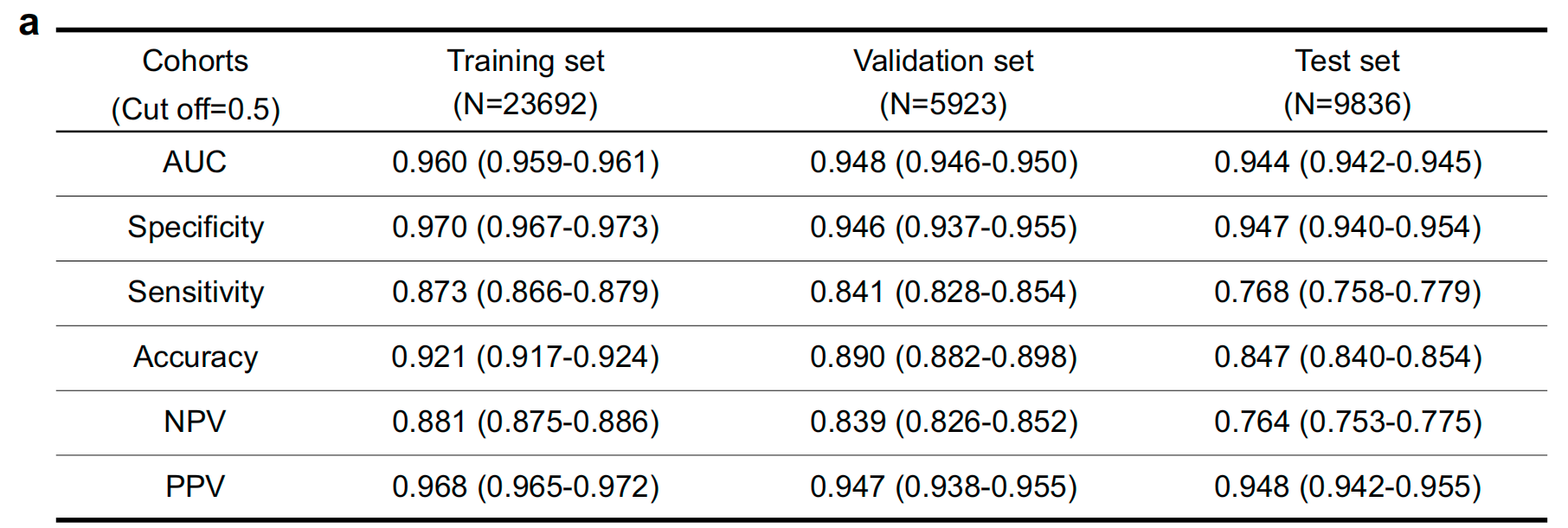
此外,在外部测试集上的AUC为 0.944(95%Cl:0.942−0.945){0.944}\left( {{95}\% \mathrm{{Cl}} : {0.942} - {0.945}}\right)0.944(95%Cl:0.942−0.945) ,准确率为 0.847(95% CI: 0.840−0.854){0.847}\left( {{95}\% \text{ CI: }{0.840} - {0.854}}\right)0.847(95% CI: 0.840−0.854) 。
在比较测试中,LLNM-Net(准确率 =0.875= {0.875}=0.875 )显著高于人类专家的预测准确率(准确率 = 0.643,配对 ttt 检验, t=1.998,P=0.0473t = {1.998},P = {0.0473}t=1.998,P=0.0473 )(图3a,b)。
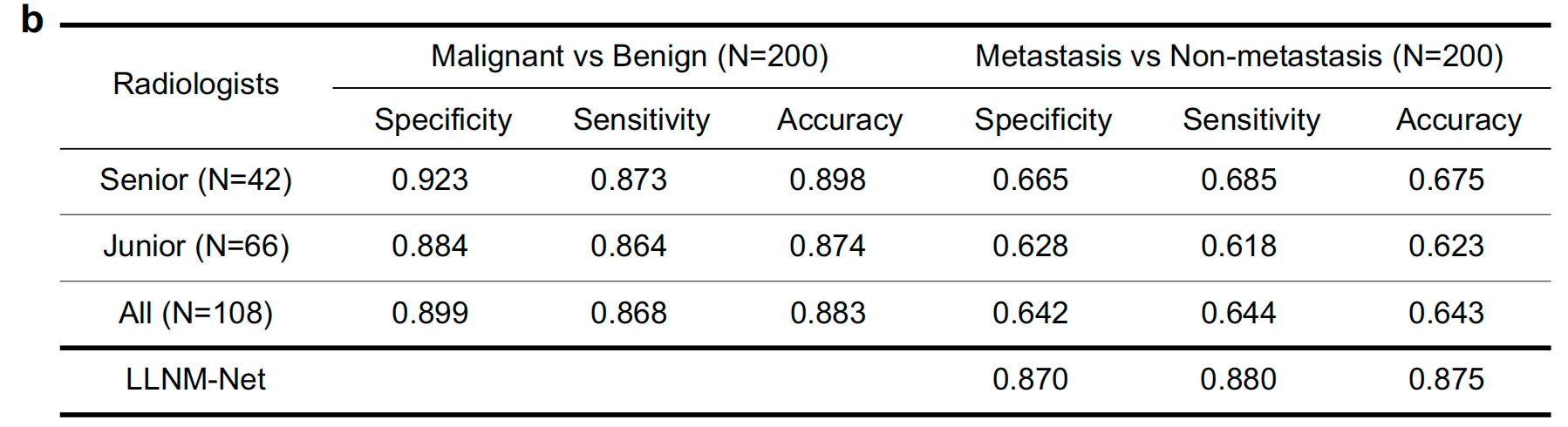
此外,结果中显示的高特异性和阳性预测值可以更有效地防止漏诊,并提高LLNM的筛查性能。
分割模块的准确率在表S4中给出,FTC和MTC的准确率结果可在表S5中找到。与最新发表的人工智能方法的比较实验结果在表S7中提供。
该研究招募了108名影像专家,其中包括42名资深放射科医生(拥有超过五年临床经验,21名女性和21名男性)和66名初级放射科医生(拥有三至五年临床经验,33名女性和33名男性)。
这些医生在诊断甲状腺结节的恶性程度方面表现出很高的准确性(图3b),平均准确率为0.883,特异性为0.899,敏感性为0.868。然而,在预测侧方淋巴结转移(LLNM)分类的实验中,资深和初级医生的预测能力都较低,准确率为0.643,特异性为0.642,敏感性为0.644(图3b、c)。
这表明基于传统临床知识和主观经验预测LLNM的能力是有限的,而人工智能模型可以从大量特征中学习有助于LLNM的重要因素。
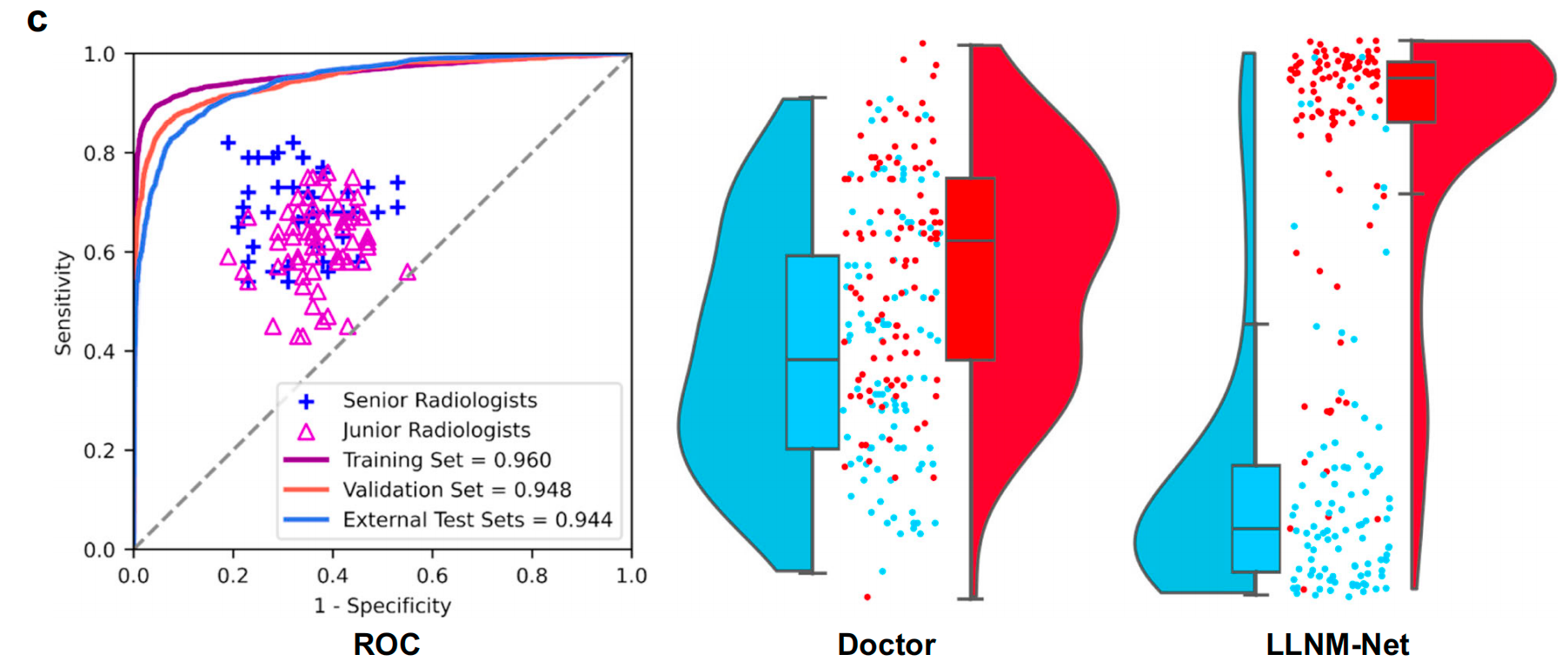
注意(图3C)
LLNM-Net在训练集、验证集和外部测试集上的受试者工作特征曲线(ROC),以及资深与初级放射科医师的预测性能对比。
曲线下面积(AUC)结果以均值呈现,95%置信区间来自每组实验设置n=100次的重复实验。每次重复试验中,真实患者输入数据通过自助采样法从真实数据集中选取。
作者采用双样本双侧未校正的Kolmogorov-Smirnov(KS)拟合优度检验来评估放射科医师与LLNM-Net预测分布值的差异。
通过结合小提琴图与箱线图的雨云图展示放射科医师组(医师雨云图,108位放射科医师平均准确率,n=200)与LLNM-Net(LLNM-Net雨云图,n=200,KS=0.385,P<1×10−12)在个体层面预测概率的比较。
每个箱线图包含表示中位数和四分位距(IQR)的箱体,须线延伸至最大值和最小值且长度不超过IQR的1.5倍。红色标记代表LLNM阳性样本,蓝色则代表阴性样本。
原始数据详见源数据文件。
预测侧方淋巴结转移的定性和定量分析
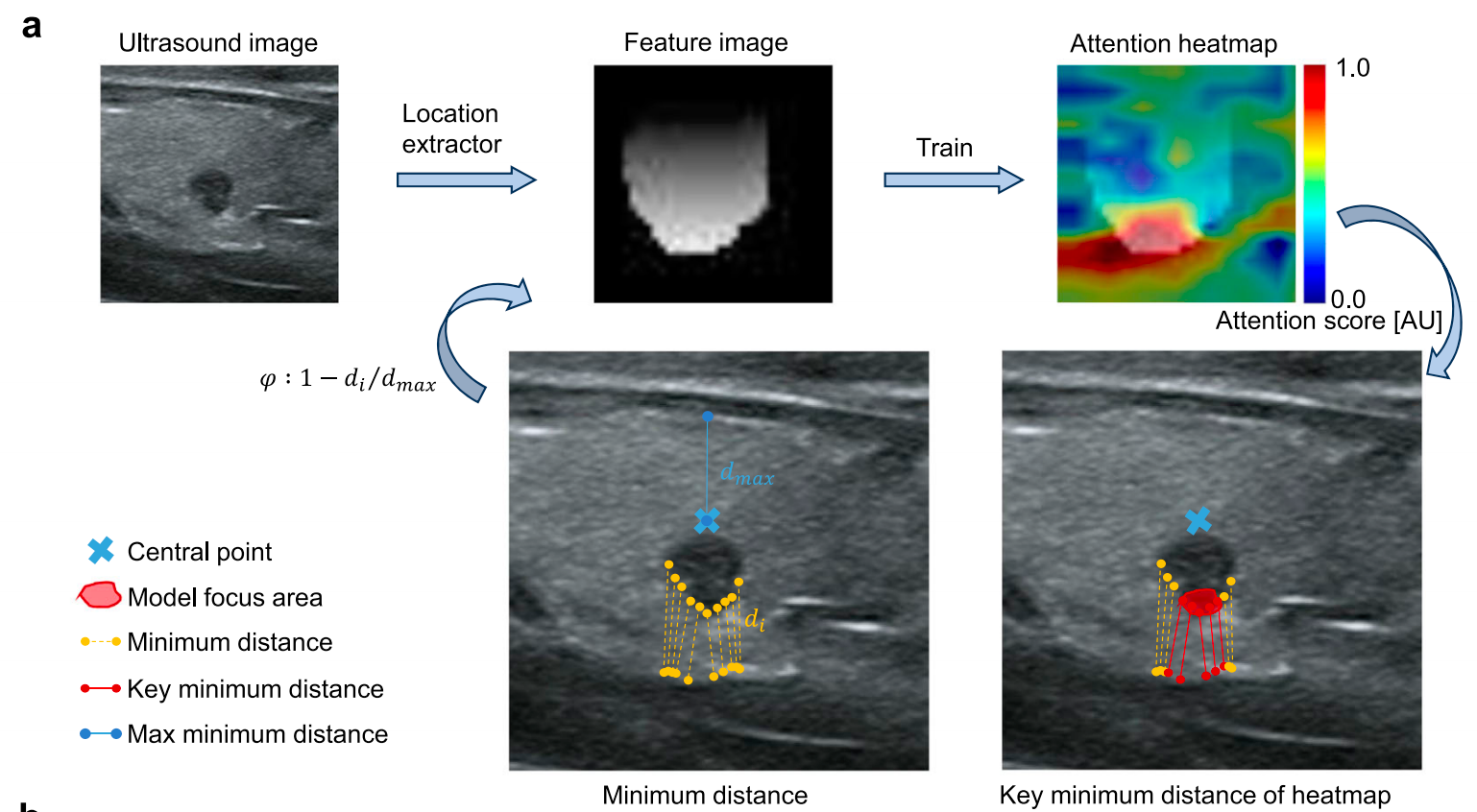
图4提供了在位置维度上预测侧方淋巴结转移的定性和定量分析。
图4a展示了结节位置信息的可视化结果。
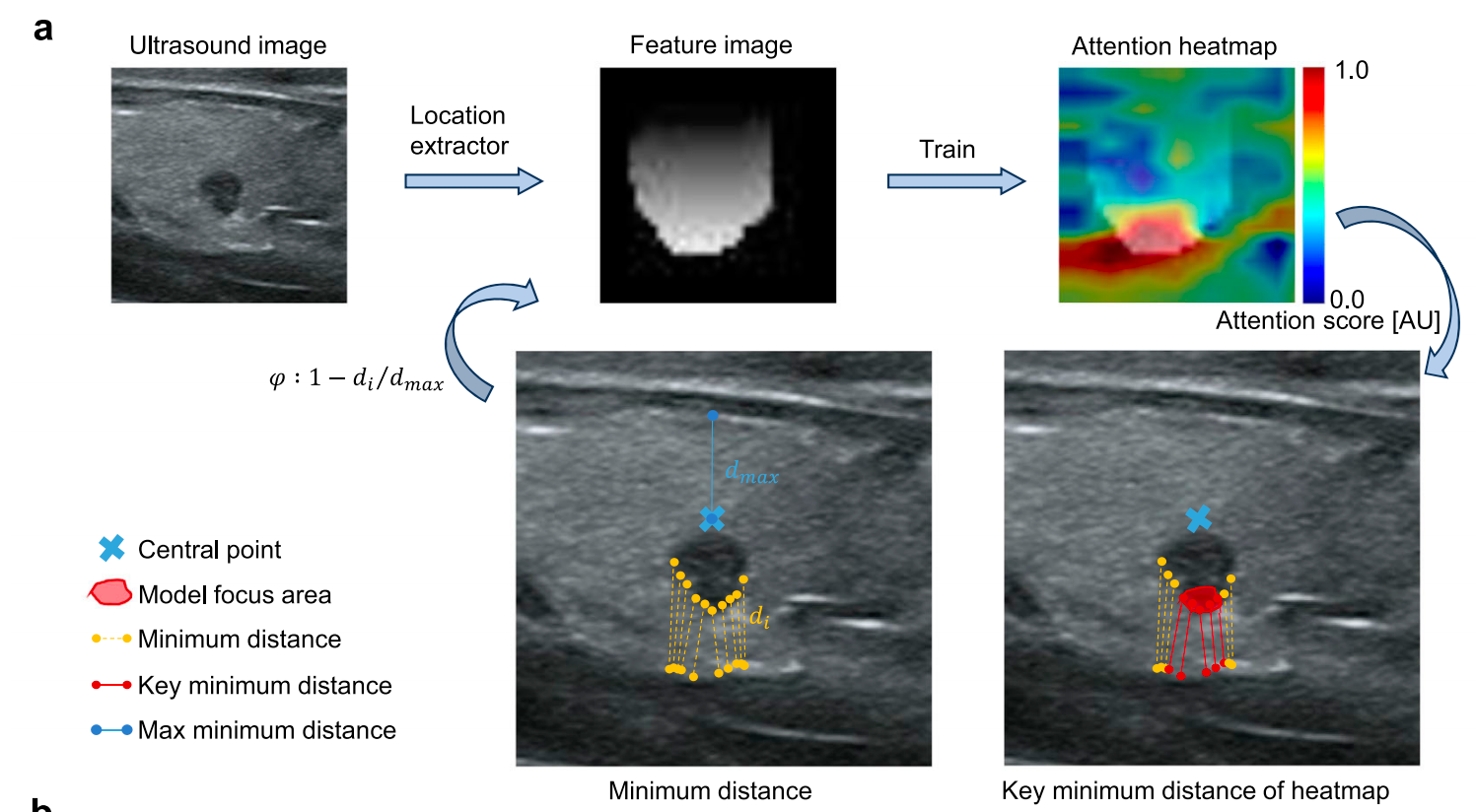
作者定义了中心点,并计算了结节区域内所有点的最小距离,通过变换 φ\varphiφ 获得位置特征图像。该模型通过梯度加权计算进行迭代学习并计算注意力热图 47{}^{47}47 ,热图指示模型识别出的对侧方淋巴结转移有较大影响的区域。
图 4 b4\mathrm{\;b}4b 展示了结节到甲状腺包膜最小距离的统计分析。
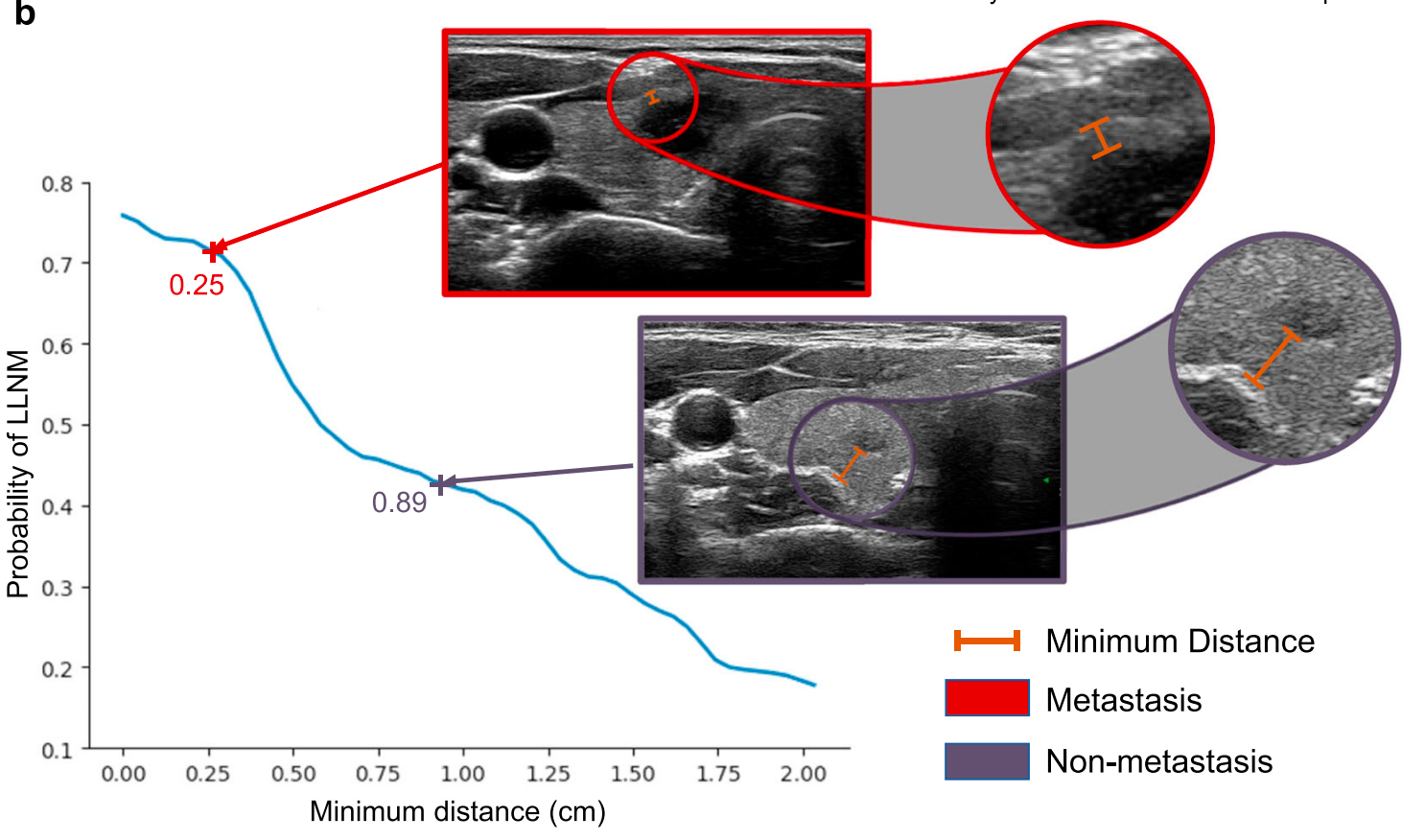
结果表明,随着最小距离减小,侧方淋巴结转移的概率相应增加。当最小距离小于 0.25 cm{0.25}\mathrm{\;{cm}}0.25cm 时,侧方淋巴结转移发生的平均概率超过 72%{72}\%72% 。
图4c展示了基于微分仿射变换方法 48,49{}^{{48},{49}}48,49 对甲状腺区域侧方淋巴结转移发生情况进行统计分析的三维风险热图模型。
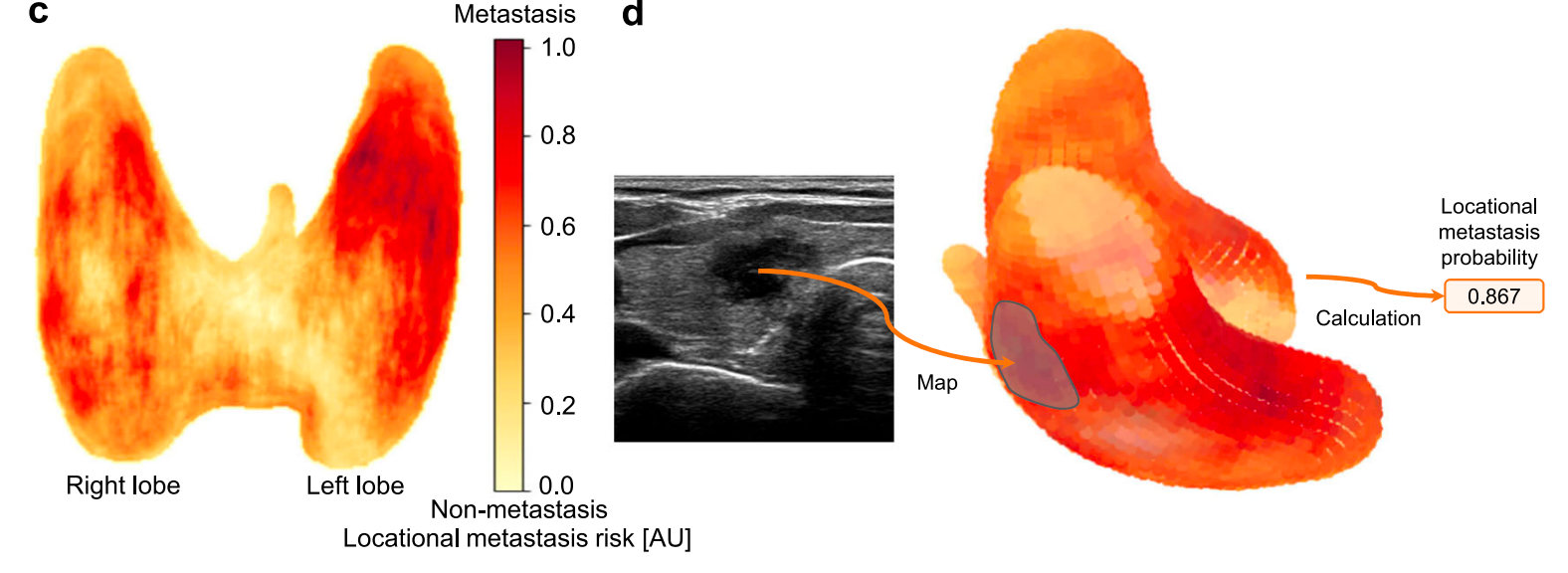
该模型可在以下网址公开获取:https://snowinbio.github.io/LLNM-Net/。
在图5中,作者展示了LLNM-Net的一个示例。
该模型将成像数据和用户信息都作为输入,并自动输出一个多特征分数。它还提供每个特征的贡献率,如右侧的桑基图所示。这个多特征转移分数有助于医生理解模型是如何预测转移的。
为了证明作者的解释与临床知识相符,作者将其与TIRADS进行了比较。可以得出结论,肿瘤恶性程度与LLNM之间存在相关性,如图S1、S2所示。
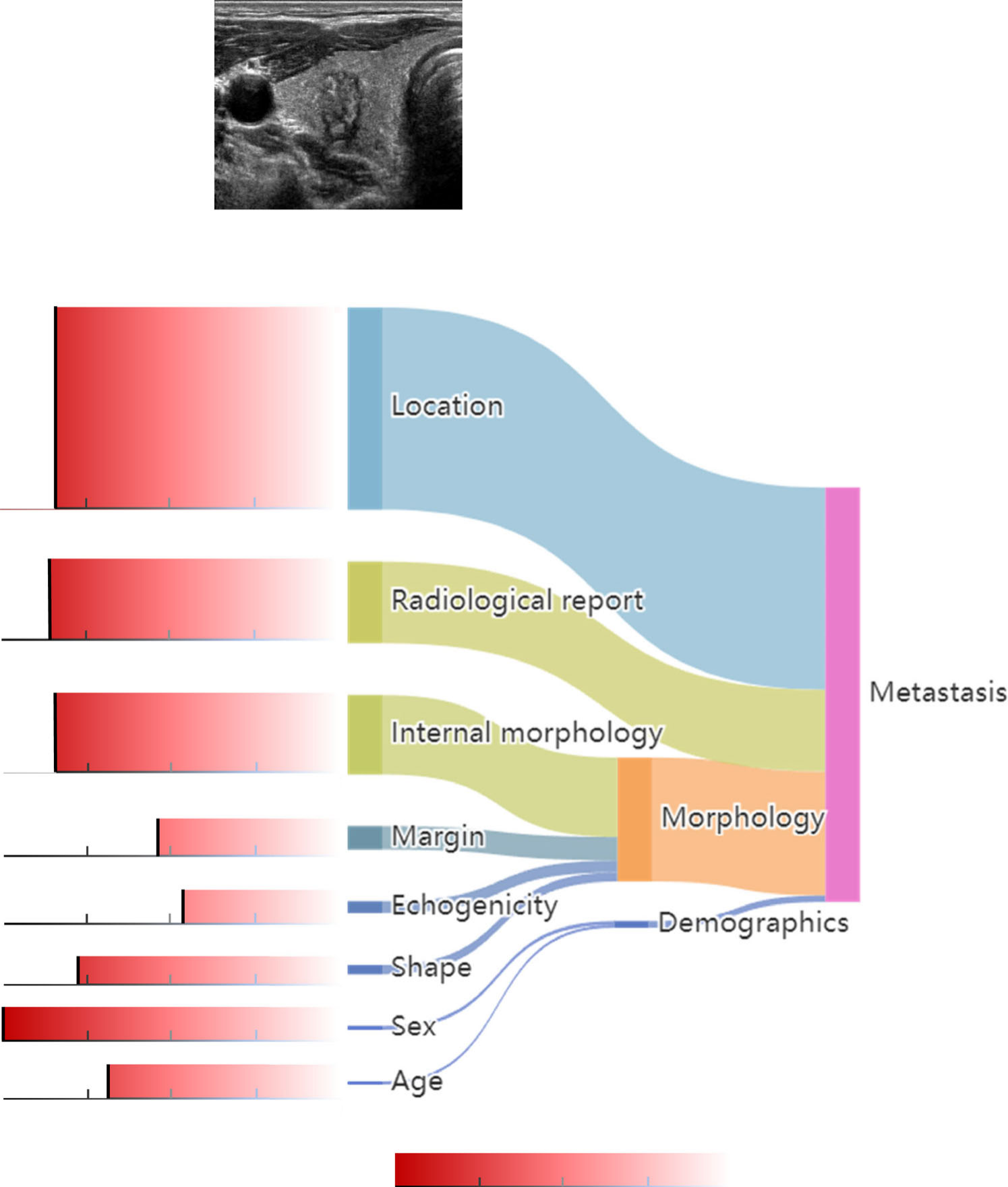
图6a显示了所有特征对LLNM的贡献率,表明甲状腺结节的生长位置是最显著的因素,占48.8%。其次是形态特征,占29.9%。
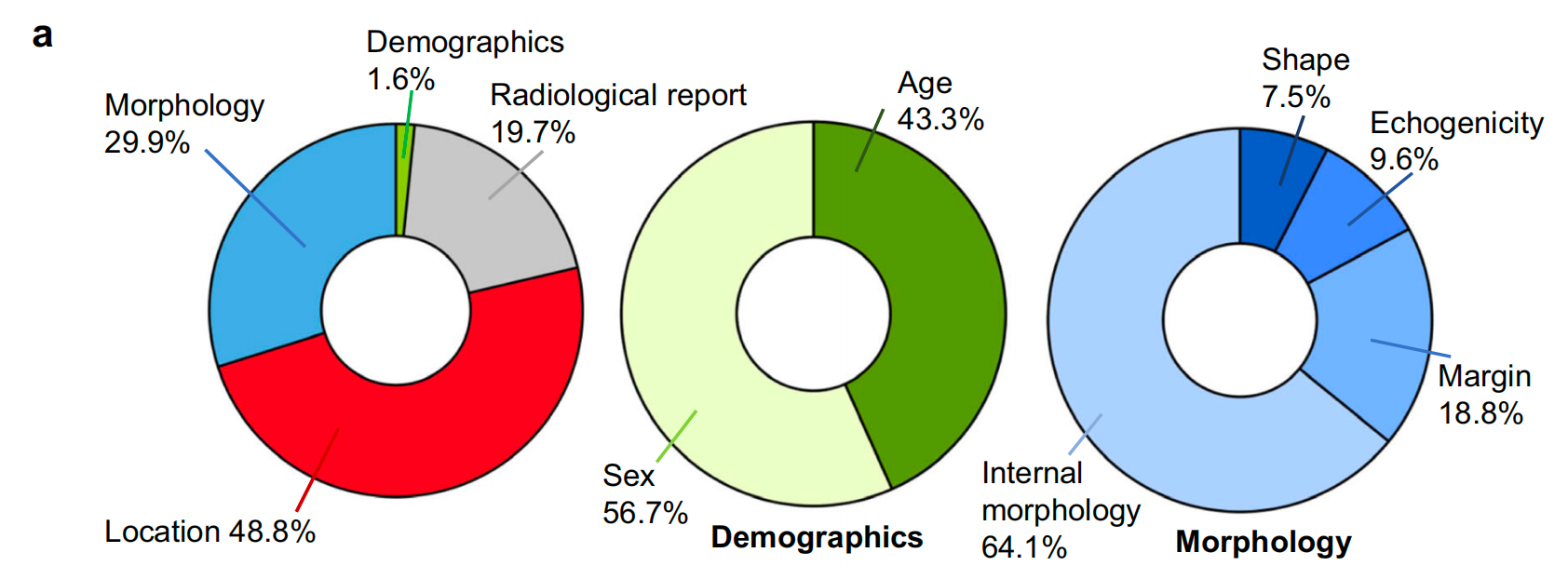
在形态特征中,形状和内部形态分别贡献7.5%和64.1%,这表明临床应关注形状异常或明显增大的结节。临床报告中的文本信息总体贡献为19.7%{19.7}\%19.7%。
性别是人口统计学中的一个重要因素(在人口统计学中占56.7%)。图6b展示了LLNM阴性和阳性病例的注意力热图,表明网络关注边缘和各种内部纹理特征。
图S3说明了成像报告与内部形态特征之间关联的示例。
决策曲线分析(图6c)说明了该策略的临床益处(有效的侧方淋巴结清扫术的益处减去侧方淋巴结清扫术的成本)。
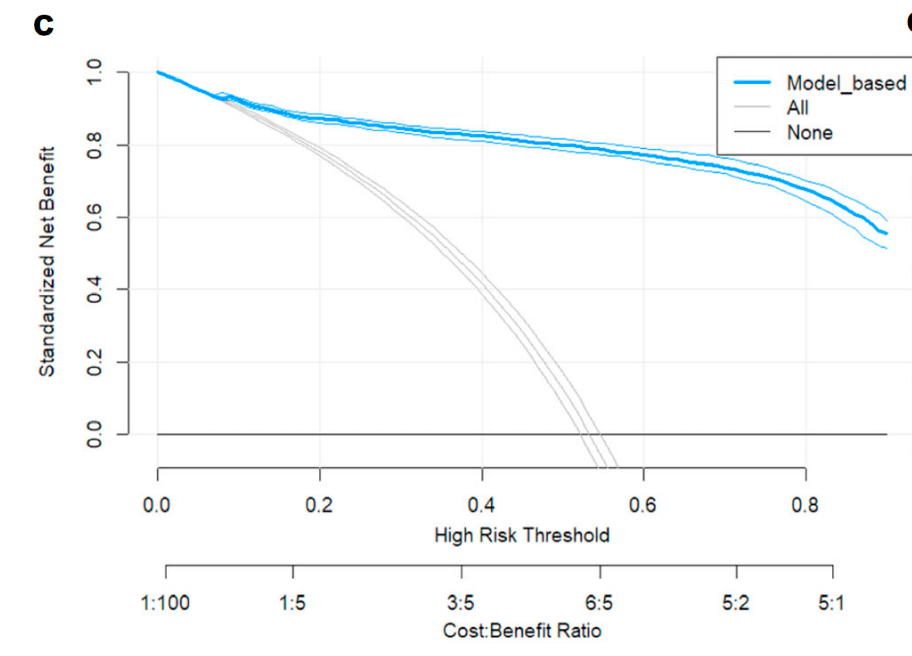
在不同的成本效益比设置下,作者基于模型的策略优于对所有患者或不对任何患者进行侧方淋巴结(LLN)细针穿刺活检(FNA)的简单策略。
图6d显示了基于模型的策略在队列中的临床影响。
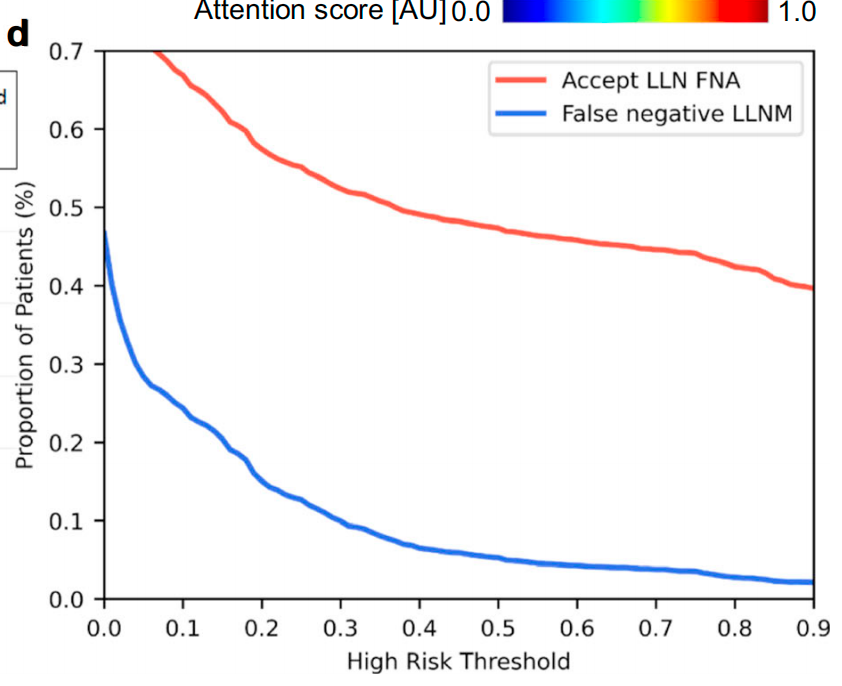
在阈值为0.5时,该策略提高了对47.4%应接受LLN FNA患者的识别率,只有5.3%的LLNM阴性患者接受了不必要的LLN FNA。
此外,作者进行了反向认知测试以评估作者模型的可解释性。结果表明,与一般人工智能相比,临床医生对模型结果的理解提高了25.4%(图S4)。
预测高危淋巴结转移患者
该模型能够预测侧方淋巴结转移的阶段。根据临床指南 3,50−52{}^{3,{50} - {52}}3,50−52 ,作者根据转移淋巴结的数量和大小将淋巴结转移分为三个阶段:
- 1期:低风险。最大直径5个或更少微转移灶 (<0.2 cm( < {0.2}\mathrm{\;{cm}}(<0.2cm 。
- 2期:中度风险。超过5个转移淋巴结,且任何转移淋巴结 <3 cm< 3\mathrm{\;{cm}}<3cm 最大直径。
- 3期:高风险。任何转移淋巴结 >3 cm> 3\mathrm{\;{cm}}>3cm 最大直径。
表2表明该模型具有良好的预测性能,在外部测试集中平均AUC为0.971。
这表明LLNM-Net可以精确识别中度至高度风险的个体,为医生提供FNA检测的参考建议,并确保对低风险个体进行定期随访,从而优化医疗资源的有效分配。
三、LLNM-Net在临床实践中的应用
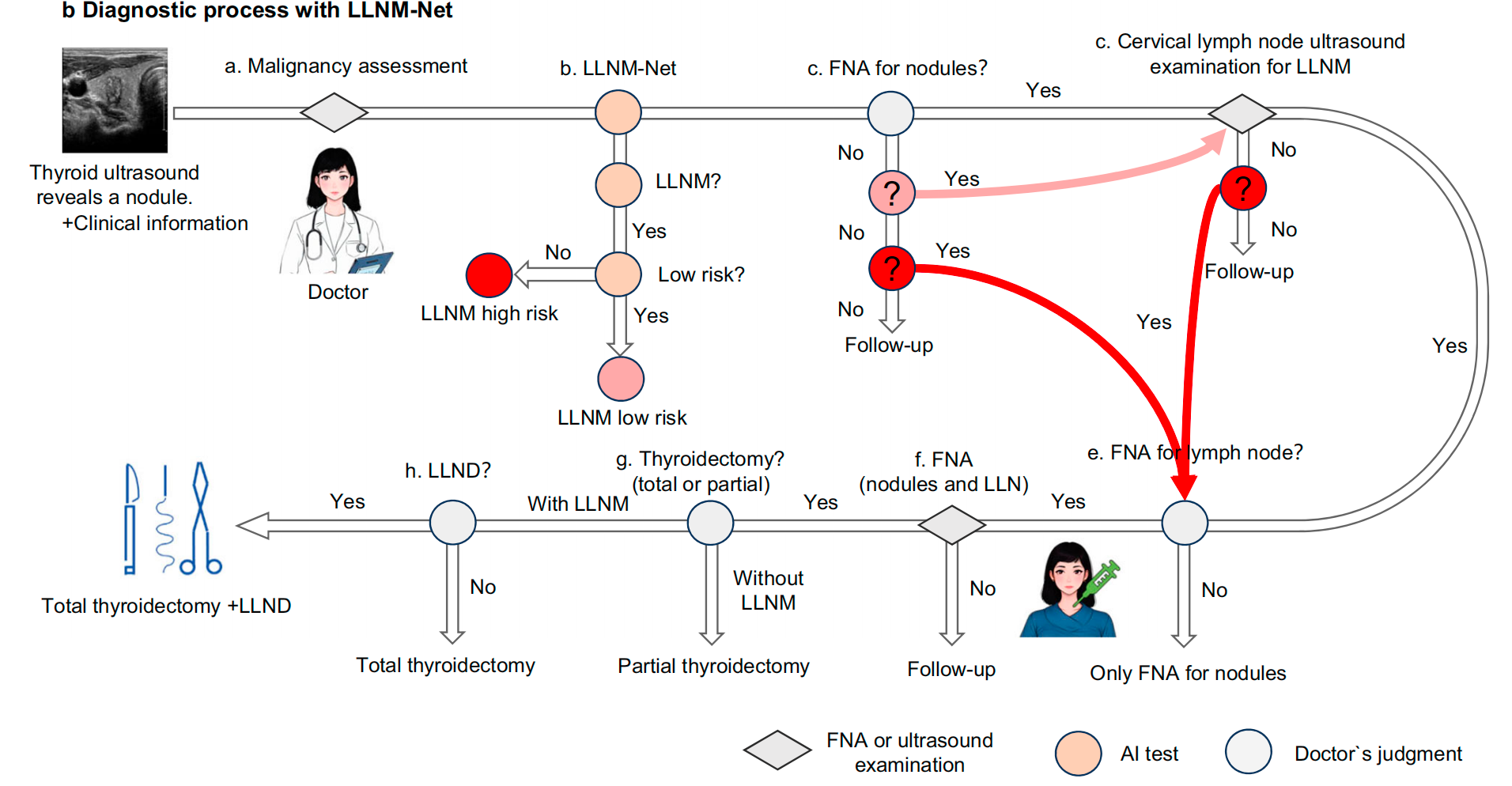
图7展示了传统临床指南 3{}^{3}3 以及结合LLNM-Net的指南。
在图7a中,当患者进行甲状腺成像时,医生基于主观经验评估结节的恶性程度,并决定是否需要进行细针穿刺抽吸活检(FNA)。
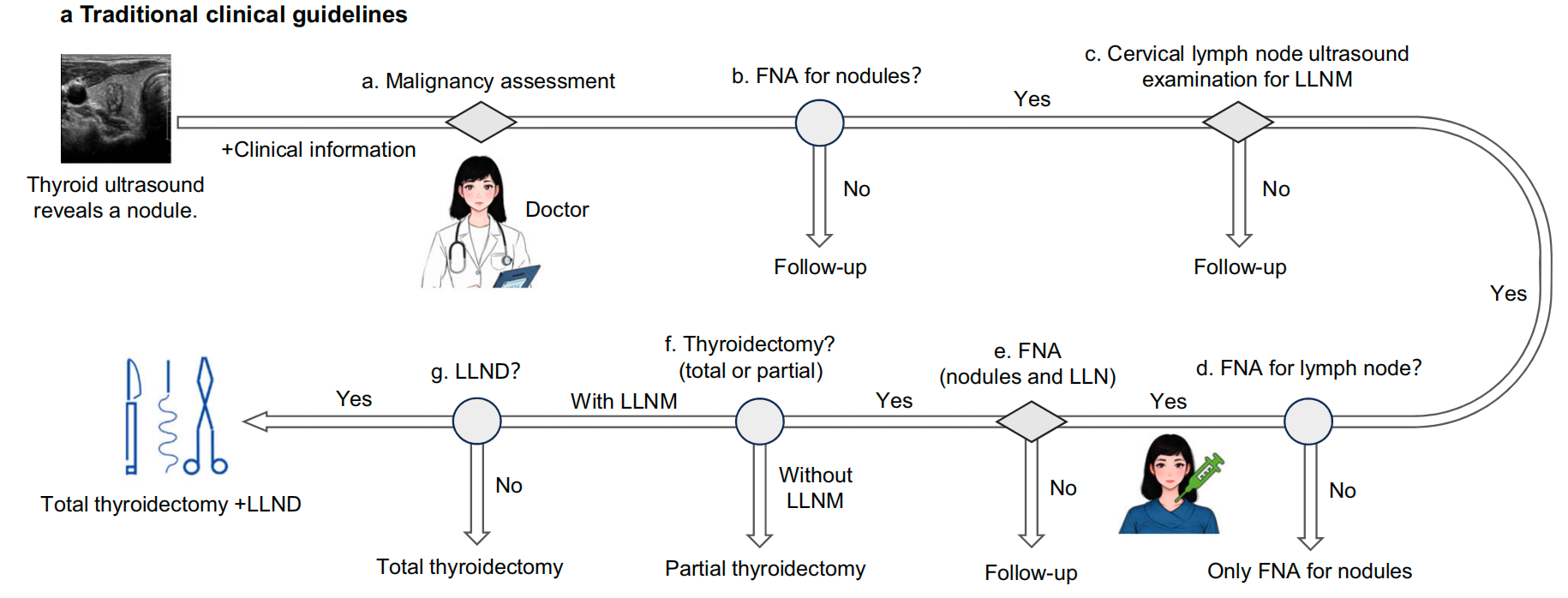
如有需要,则考虑进行颈部淋巴结超声检查,以评估侧方淋巴结转移(LLNM)的可能性,并决定是否对侧方淋巴结进行FNA。然后根据FNA结果决定是否进行甲状腺切除术和侧方淋巴结清扫术(LLND)。
然而,医生是否进行颈部超声检查取决于主观经验,这可能导致潜在的漏诊。超声检查过程中检测区域覆盖不完整也可能导致漏诊,影响淋巴结FNA结果的准确性,并影响是否进行LLND的决策。
在图7b中,LLNM-Net的整合有助于术前LLNM风险预测,帮助医生确定是否进行颈部超声检查,从而减少漏诊。
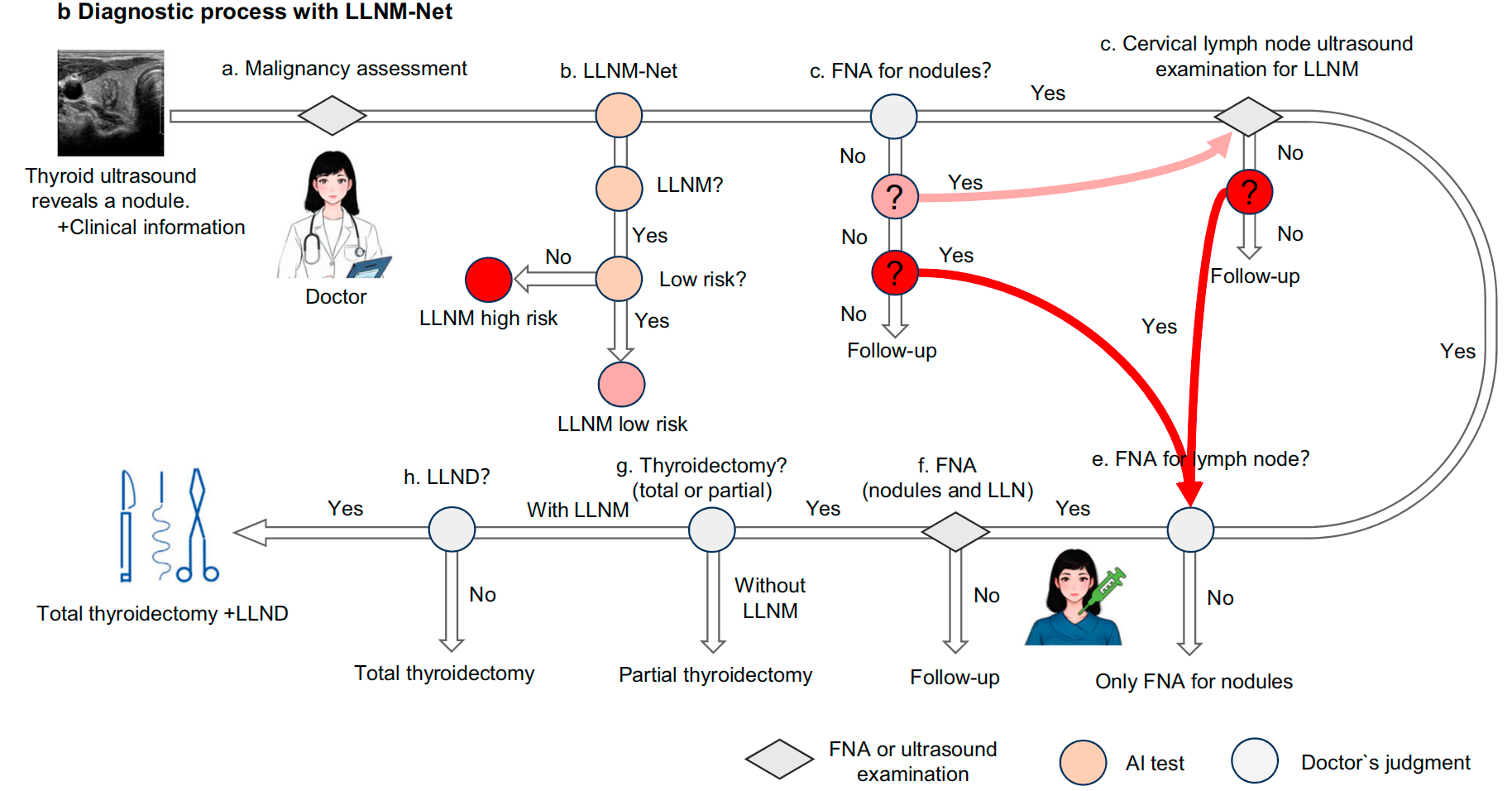
在这项诊断研究中,作者开发了一种可解释的多模态深度学习模型,该模型可以作为基于甲状腺超声图像的LLNM风险评估的人工智能支持系统来实施。
该模型基于融合变压器方法为预测提供定性和定量的临床解释。
本研究解决了术前诊断LLNM缺乏有效方法的问题,在准确筛查高危人群的同时提供临床见解,并显著提高患者生存率和社会福利。
四、讨论
作者开发了LLNM-Net,实现了对LLNM的精确术前预测,并在五个外部中心展示了强大的泛化能力,预测性能的曲线下面积(AUC)达到0.944(95%置信区间:0.942 - 0.945)。
目前,超声检测侧颈部区域的灵敏度较低,为0.623。作者的模型的AUC比现有最佳模型提高了7.4%,其准确性比人类医生高 20.4%{20.4}\%20.4% 。在高危人群筛查中,AUC达到0.971。
作者的研究为临床检测区域研究提供了指导,揭示了以下发现:位于左叶中上区域和右叶中上区域的结节是LLNM的高危区域,这表明临床医生应关注这些区域。这可能与淋巴转移途径密切相关。
统计数据表明,当结节与包膜之间的最小距离小于 0.25 cm{0.25}\mathrm{\;{cm}}0.25cm 时,LLNM的平均概率超过72%,这表明最小距离、生长区域与LLNM之间存在关联。作者对每位患者的风险区域和特征贡献进行了量化。
作者通过使用基于注意力的前景优化分割网络来精确分割结节,解决了超声图像中前景小和背景类内方差高的挑战。
为了解决超声图像中的多尺度问题,作者提出了一种CPDT方法来准确提取甲状腺结节的精确位置信息。
为了有效整合超声图像和临床信息,作者设计了一种基于双向注意力交换机制的多模态深度学习方法,提取报告文本和影像特征之间的局部互联信息,并揭示临床医生的潜在发现。
这种端到端的多模态特征提取方法可广泛应用于高效的肿瘤检测、生长位置分析和性质评估,有潜力解决各种疾病中的大多数影像诊断任务。
在传统诊断过程中,医生依靠主观经验来决定是否进行颈部超声检查,这可能导致潜在的漏诊。
在颈部超声检查过程中,检测区域覆盖不完整也可能导致漏诊,影响淋巴结细针穿刺抽吸(FNA)结果的准确性,并影响侧方淋巴结清扫(LLND)的决策。
使用LLNM-Net可以通过帮助降低颈部超声的漏检率,并最大限度减少因检查区域不完整导致的漏诊,从而优化这一过程,进而改进临床指南。
作者的研究仍存在一些局限性。首先,收集的病例数量和疾病类型有限。未来,作者计划从更广泛的人群中收集更丰富的数据,包括更多亚型、国家和地区,以提高LLNM-Net的通用性和适用性。
其次,作者模型的实际临床效益尚未得到验证。作者计划设计前瞻性实验进行验证,并探索该模型在不同机构和地区的实际效果。
结束语
本期推文的内容就到这里啦,如果需要获取医学AI领域的最新发展动态,请关注小罗的推送!如需进一步深入研究,获取相关科研服务,欢迎扫码前往我们团队的主页!

魔乐社区(Modelers.cn) 是一个中立、公益的人工智能社区,提供人工智能工具、模型、数据的托管、展示与应用协同服务,为人工智能开发及爱好者搭建开放的学习交流平台。社区通过理事会方式运作,由全产业链共同建设、共同运营、共同享有,推动国产AI生态繁荣发展。
更多推荐
 已为社区贡献1条内容
已为社区贡献1条内容







所有评论(0)