14分Top刊NC代码开源|NSCLC单细胞+空转肿瘤微环境分析
肺癌是全球第二大最常见的癌症,也是癌症相关死亡的主要原因。肿瘤生态系统具有多种免疫细胞类型。髓系细胞尤其普遍,并且在促进疾病方面发挥着众所周知的作用。在我们的研究中,我们通过单细胞和空间转录组学分析了 25 名未经治疗的腺癌和鳞状细胞癌患者的约 900,000 个细胞。我们注意到抗炎巨噬细胞与 NK 细胞/T 细胞之间存在反比关系,并且肿瘤内的 NK 细胞细胞毒性降低。虽然我们观察到腺癌和鳞状细胞
说在前面
说起肺癌真的过去回忆历历在目,小编毕业后职业生涯的第一个项目——非小细胞肺癌预后有效靶点筛选。当时肝的是转录组预后+建模筛选。
做研发其实要求是远远高于发文章的,文章投不出去就降分,加工作量,做药要是烂尾或者就算是有瑕疵直接寄,钱钱用之如泥沙。话不多说,欣赏一篇NSCLC的多组学分析
小编整理打包了文章多组学分析及copyKAT的代码
文末公众号后台回复20240701lung即可领取项目代码
今天给大家分享的一篇文章:Single-cell and spatial transcriptomics analysis of non-small cell lung cancer

- 标题:非小细胞肺癌的单细胞和空间转录组学分析
- 期刊名称:Nature Communications
- 影响因子:14.7
- JCR分区:1区
- 中科院分区:综合性期刊1区 Top
- 小类:综合性期刊1区
摘要
肺癌是全球第二大最常见的癌症,也是癌症相关死亡的主要原因。肿瘤生态系统具有多种免疫细胞类型。髓系细胞尤其普遍,并且在促进疾病方面发挥着众所周知的作用。在我们的研究中,我们通过单细胞和空间转录组学分析了 25 名未经治疗的腺癌和鳞状细胞癌患者的约 900,000 个细胞。我们注意到抗炎巨噬细胞与 NK 细胞/T 细胞之间存在反比关系,并且肿瘤内的 NK 细胞细胞毒性降低。虽然我们观察到腺癌和鳞状细胞癌中的细胞类型组成相似,但我们发现各种免疫检查点抑制剂的共表达存在显著差异。此外,我们还揭示了肿瘤中巨噬细胞转录“重编程”的证据,使其转向胆固醇输出并采用促进铁流出的胎儿样转录特征。我们的多组学资源提供了肿瘤相关巨噬细胞的高分辨率分子图谱,增强了我们对其在肿瘤微环境中的作用的理解。
结果
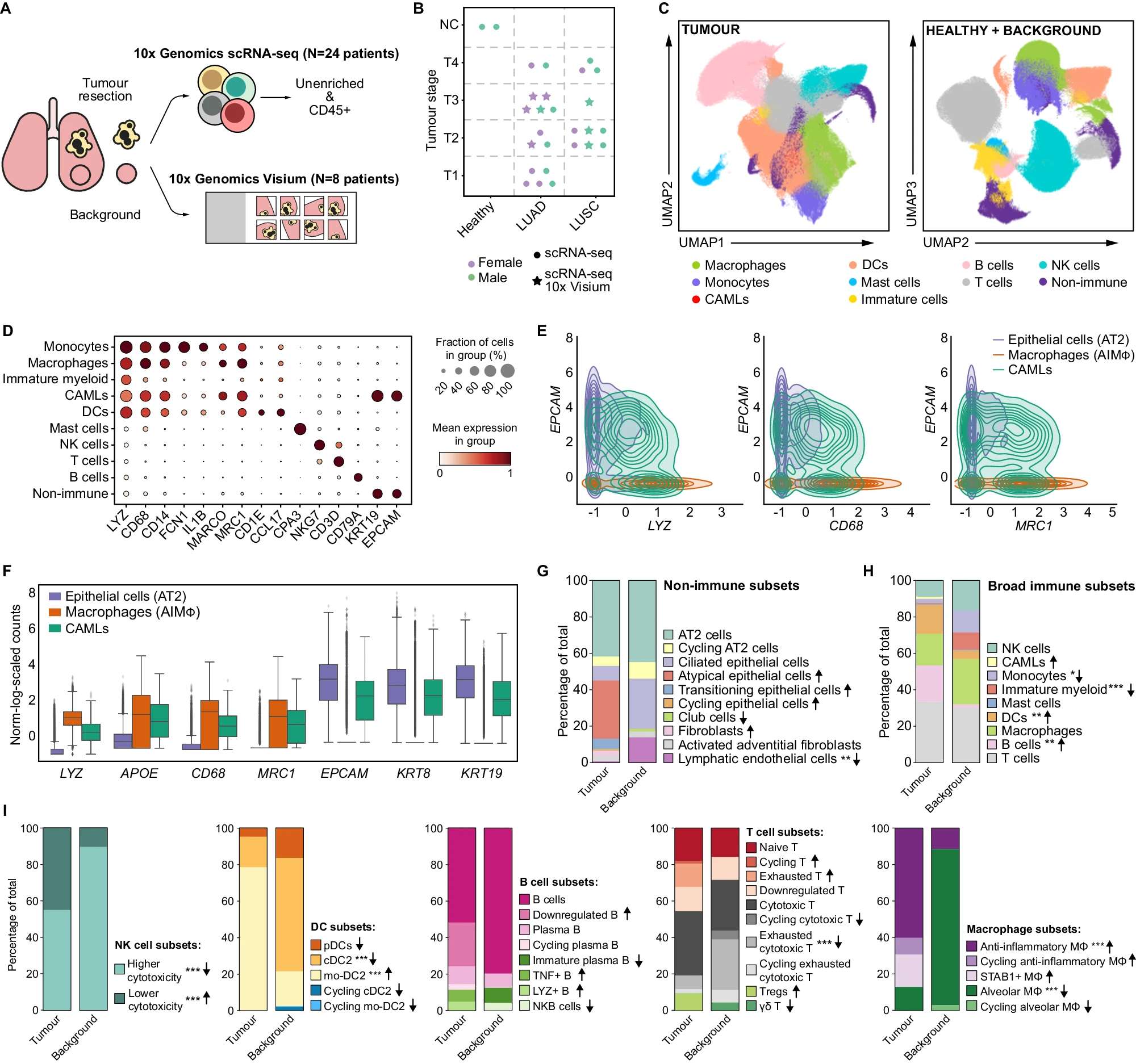
- A 研究概览。采用CD45+或CD235−富集的方法对切除的肿瘤组织、相邻的非肿瘤组织(背景)和健康肺部的单细胞悬液进行了单细胞RNA测序(scRNA-seq)。使用新鲜、急速冷冻的肿瘤、背景和健康组织的冷冻切片进行了10x Visium空间转录组学研究。
- B 队列概览。符号代表单个病人和进行的分析。
- C UMAP投影显示肿瘤和结合的背景+健康数据集。
- D 肿瘤样本中用于广泛细胞类型注释的代表性基因的点图。
- E 等高线图展示AT2细胞(44,399个细胞)、CAMLs(2,520个细胞)和AIMɸ(16,120个细胞)中髓系(LYZ, CD68, MRC1)和上皮(EPCAM)基因的共表达。标准化、缩放和对数变换后的基因表达。
- F 盒形图展示AT2细胞、CAMLs和AIMɸ中髓系(LYZ, APOE, CD68, MRC1)和上皮(EPCAM, KRT8, KRT19)基因的标准化、缩放和对数变换后的基因表达。
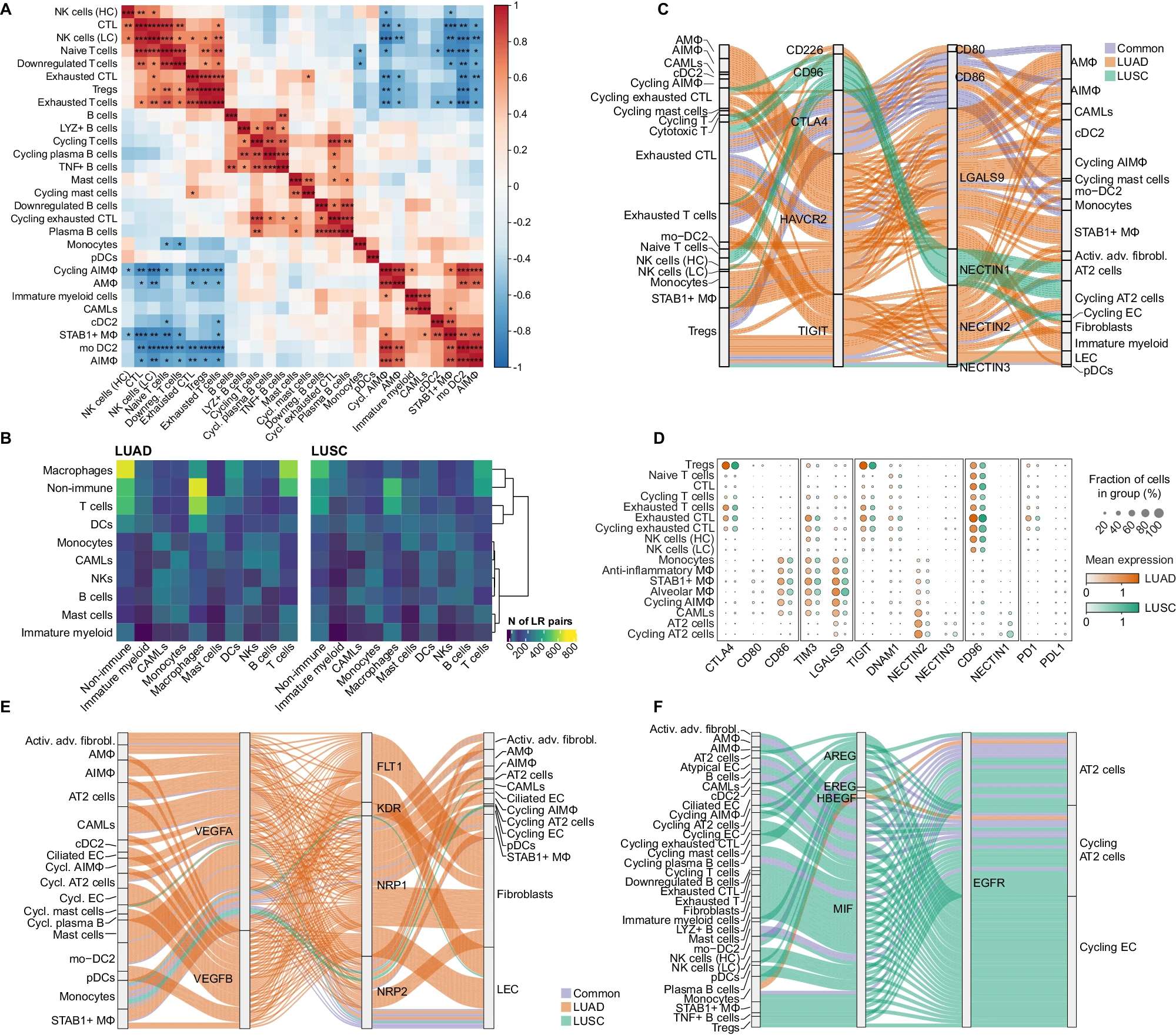
- A 热图显示了每种免疫细胞类型(在CD235−富集中计算得到的)相对细胞类型丰度之间的皮尔逊相关系数。颜色表示皮尔逊相关系数值,星号表示双侧关联测试的显著性水平,该测试基于皮尔逊乘积矩相关系数计算。
- B 热图显示LUAD(左)和LUSC(右)中所有细胞类型之间的LR(配体-受体)相互作用次数,通过广泛的细胞注释进行总结。行使用欧几里得距离的完全连接方法进行了层次聚类。
- C Sankey图显示了cellphoneDB检测到的LUAD和LUSC中选定的ICI(免疫检查点抑制剂)的肿瘤特异性相互作用。线条颜色标识每种细胞类型之间的LR相互作用是仅在LUAD中发现(橙色)、仅在LUSC中发现(绿色)还是在两种肿瘤类型中都有(蓝色)。
- D 点图显示了©中突出显示的ICI基因和细胞类型,按肿瘤类型分开。每个点的大小代表该簇中表达该基因的细胞百分比,而颜色表示每组中每个基因的平均标准化缩放对数变换表达量。
- E Sankey图显示了cellphoneDB检测到的LUAD和LUSC中VEGFA/B相互作用者的肿瘤特异性相互作用。线条颜色标识每种细胞类型之间的LR相互作用是仅在LUAD中发现(橙色)、仅在LUSC中发现(绿色)还是在两种肿瘤中都有(蓝色)。
- F Sankey图显示了cellphoneDB检测到的LUAD和LUSC中EGFR相互作用者的肿瘤特异性相互作用。线条颜色标识每种细胞类型之间的LR相互作用是仅在LUAD中发现(橙色)、仅在LUSC中发现(绿色)还是在两种肿瘤中都有(蓝色)。
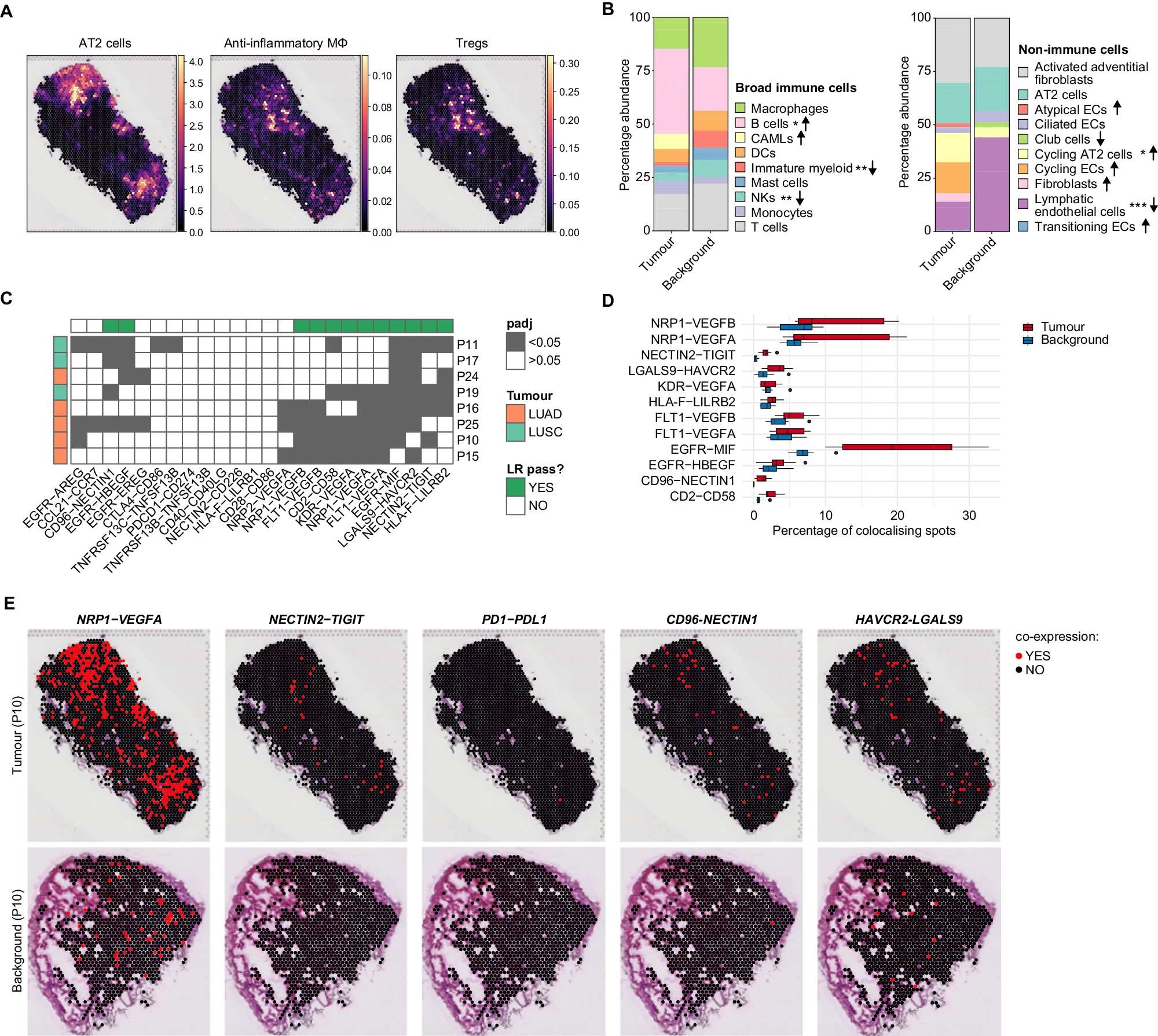
- A 空间图像展示了用cell2location估计的代表性肿瘤切片上AT2细胞、AIMɸ和Tregs的细胞丰度。
- B 使用cell2location对肿瘤和背景切片的细胞丰度估计,计算了免疫(左侧)和非免疫(右侧)细胞类型的相对比例。免疫细胞按照宽泛的注释分组。箭头表示与背景相比,在肿瘤中的增加(↑)或减少(↓)。使用双侧Wilcoxon秩次检验和Bonferroni校正进行了成对比较。
- C 空间LR共定位的热图。在每个斑点上估计了所有切片的LR基因对共表达,使用χ2检验并随后进行Bonferroni多重比较校正,比较了肿瘤和背景中共定位与非共定位斑点的频率。深灰色砖块表示肿瘤和背景切片中共定位基因对的频率显著不同。绿色列注释表示至少在八个病人中四个以上的LR对显著。行注释指示肿瘤类型。
- D 盒形图显示在每个分析的切片中,共定位LR对在肿瘤与背景间频率显著不同的情况。N=8个病人。盒形图使用Python Seaborn包的默认设置绘制,即盒子显示四分位数,胡须长度是四分位距的1.5倍。源数据提供为源数据文件。
- E 空间图像展示了在肿瘤(顶部)和背景(底部)中发现LR对共表达的斑点的位置,对于NRP1-VEGFA, NECTIN2-TIGIT, PD1-PDL1, CD96-NECTIN1 和 HAVCR2-LGALS9。来自一位病人的代表性切片。
-
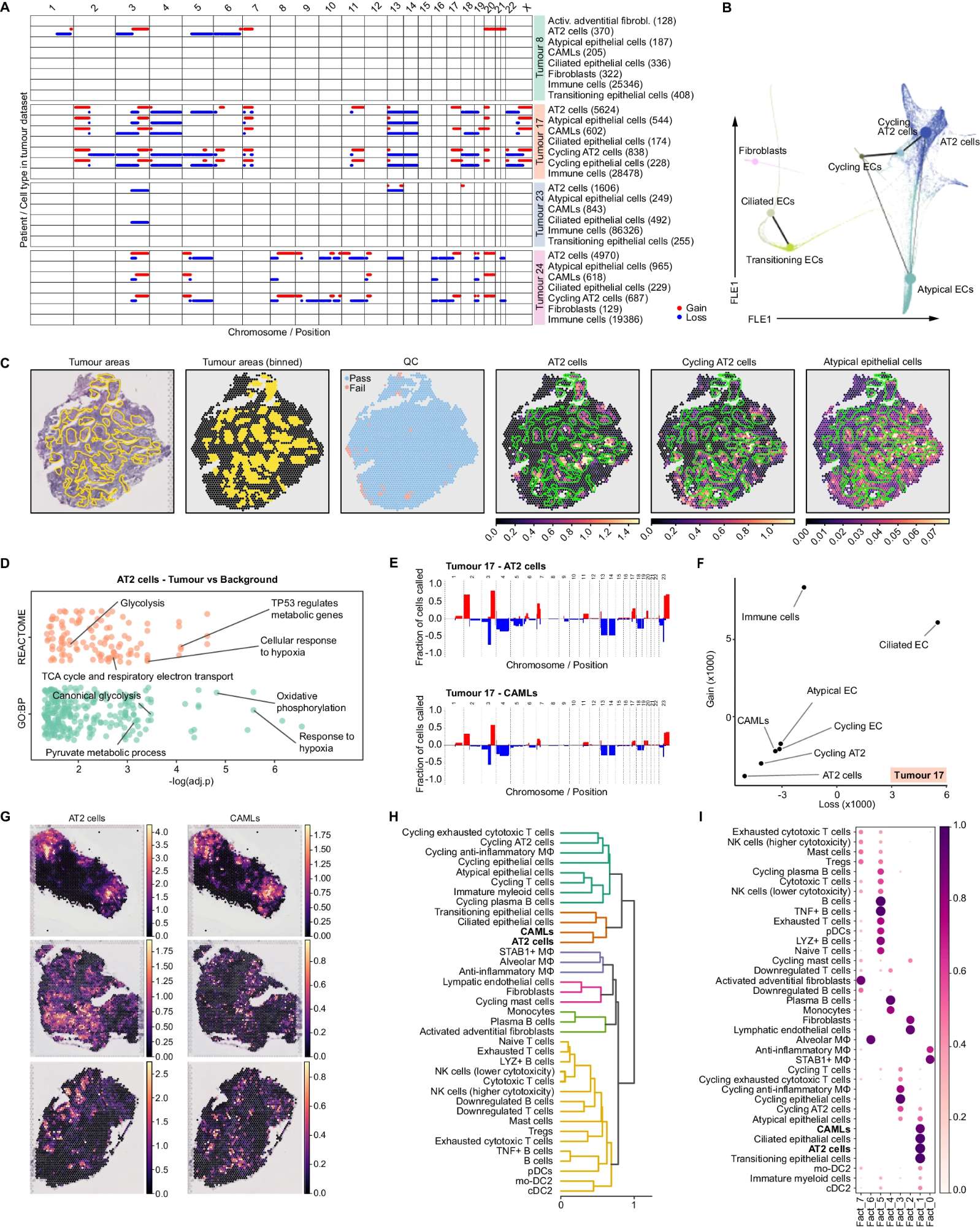
A CNA分析: 图表展示了通过CopyKat估计的每个染色体臂上不同细胞类型和患者的染色体增益(红线)和损失(蓝线)。所有免疫细胞类型为绘图目的被分组在一起。
-
B PAGA图层:在肿瘤中非免疫细胞类型的扩散图(FLE嵌入)上叠加PAGA图。
-
C 盲注释:前三个面板—资深病理学家标注的肿瘤浸润区域(左),Visium点上的肿瘤区域分桶(中)和通过QC的点(右)。后三个面板—在同一切片上的cell2location估计的AT2细胞(左)、周期性AT2细胞(中)和非典型上皮细胞(右),叠加了病理学家对肿瘤浸润的注释(绿色轮廓)。
-
D 基因本体和REACTOME数据库的超表达分析:使用clusterProfiler R包,基于AT2细胞在肿瘤与背景中上调的差异表达基因(DEGs),对生物过程进行超表达分析。提供源数据文件。
-
E 一个代表性患者肿瘤中AT2和CAMLs的CNA详细概览:条形图显示特定染色体区域中携带染色体增益(红色条)或损失(蓝色条)的细胞频率。
-
F 散点图显示KL散度:用于计算肿瘤数据集中每种细胞类型的增益和损失分布之间的KL散度,损失在x轴,增益在y轴。所有免疫细胞类型为绘图目的被分组在一起。
-
G 空间图像:展示cell2location估计的三个代表性肿瘤切片上AT2细胞和CAMLs的细胞丰度。
-
H 层次聚类:计算通过QC的所有肿瘤切片中点的细胞类型组成(由cell2location估计)的相关距离。
-
I 非负矩阵分解:建立在通过QC的所有肿瘤切片中点的细胞类型丰度的q05估计上,使用cell2location估计。
-
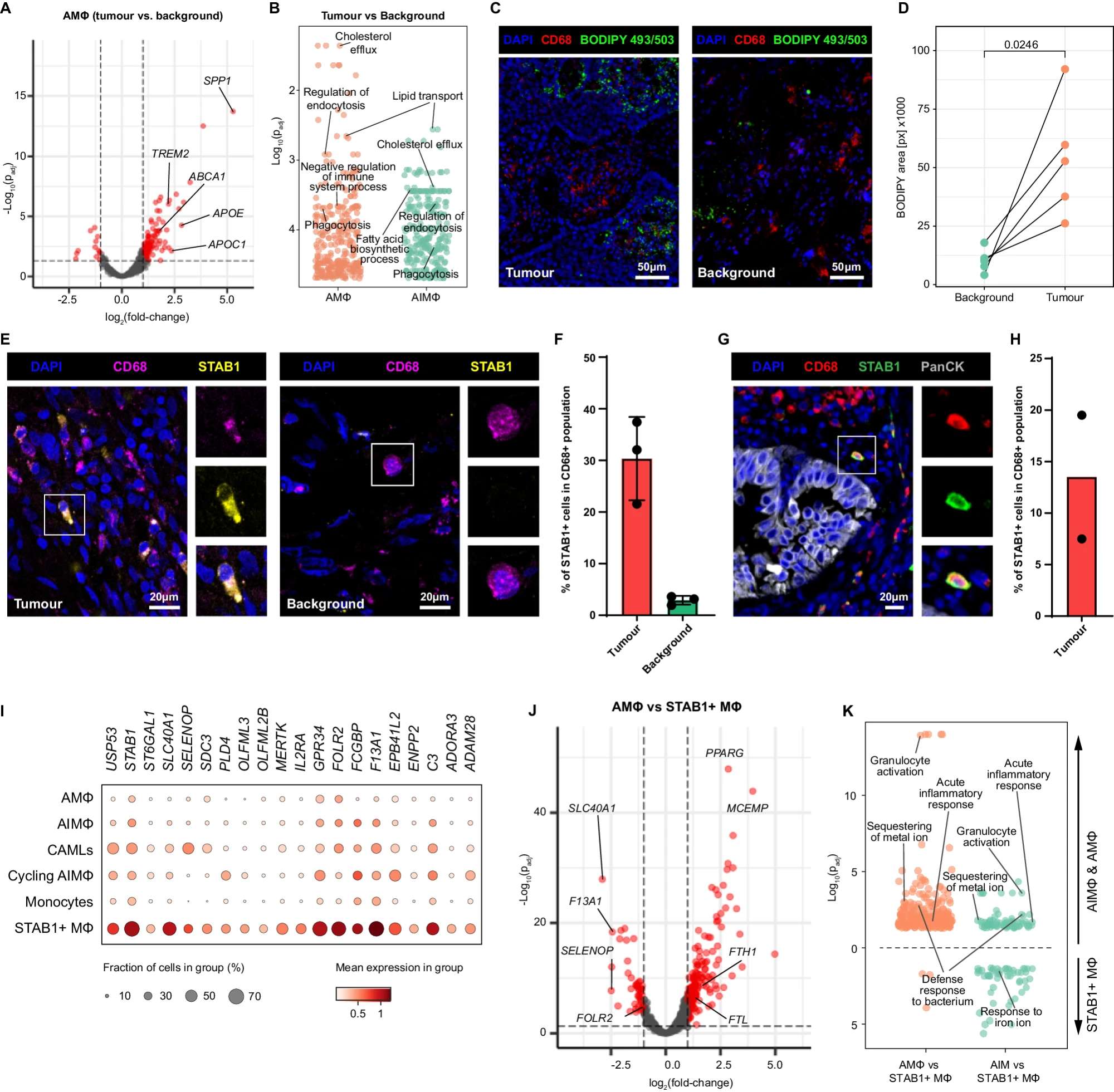
A 火山图分析:使用py_DESeq2包提取的AIMɸ在肿瘤与背景比较中的差异表达基因(DEGs,红色表示)的火山图。
-
B 基因本体超表达分析:使用clusterProfiler R包对Alveolar Mɸ和AIMɸ在肿瘤与背景中上调的DEGs进行基因本体—生物过程数据库的超表达分析。提供源数据文件。
-
C 免疫组化染色(IHC):在肿瘤和背景组织切片上对CD68和中性脂类(BODIPY 493/503)进行免疫组化染色。Z堆叠的最大强度投影。标尺为50微米。
-
D BODIPY信号覆盖面积分析:比较肿瘤与背景切片中BODIPY信号的覆盖面积,使用配对的双侧t检验,匹配同一患者的肿瘤和背景切片。N=5个患者。提供源数据文件。
-
E CD68和STAB1的免疫组化染色:在肿瘤(左)和背景(右)组织切片上进行CD68和STAB1的免疫组化染色。Z堆叠的最大强度投影。小插图显示单个细胞的详细放大。标尺为20微米。
-
F STAB1+细胞的定量:显示CD68+巨噬细胞群体中STAB1+细胞的比例,以CD68+区域的百分比表示。数据以平均值和标准偏差表示(n=3个生物重复)。提供源数据文件。
-
G CD68, STAB1和PanCK的染色:在肿瘤组织切片上进行CD68, STAB1和PanCK的染色。Z堆叠的最大强度投影。小插图显示单个细胞的详细放大。标尺为20微米。
-
H STAB1+ CD68+细胞的定量:在非小细胞肺癌(NSCLC)中,定量CD68+巨噬细胞群体中的STAB1+ CD68+细胞。数据以平均值和单个数据点表示(n=2个生物重复)。提供源数据文件。
-
I 点图:显示肿瘤中所有巨噬细胞亚群和CAMLs中的“STAB1标志基因”表达。
-
J 火山图分析:由py_DESeq2识别的Alveolar Mɸ vs STAB1 Mɸ在肿瘤中的DEGs的火山图(红色表示)。
-
K 基因本体超表达分析:使用clusterProfiler R包对Alveolar Mɸ vs STAB1 Mɸ(顶部)和AIMɸ vs STAB1 Mɸ(底部)在肿瘤中的DEGs进行基因本体—生物过程数据库的超表达分析,分别显示STAB1 Mɸ上调(左侧)和Alveolar Mɸ或AIMɸ上调(右侧)的DEGs。提供源数据文件。
-
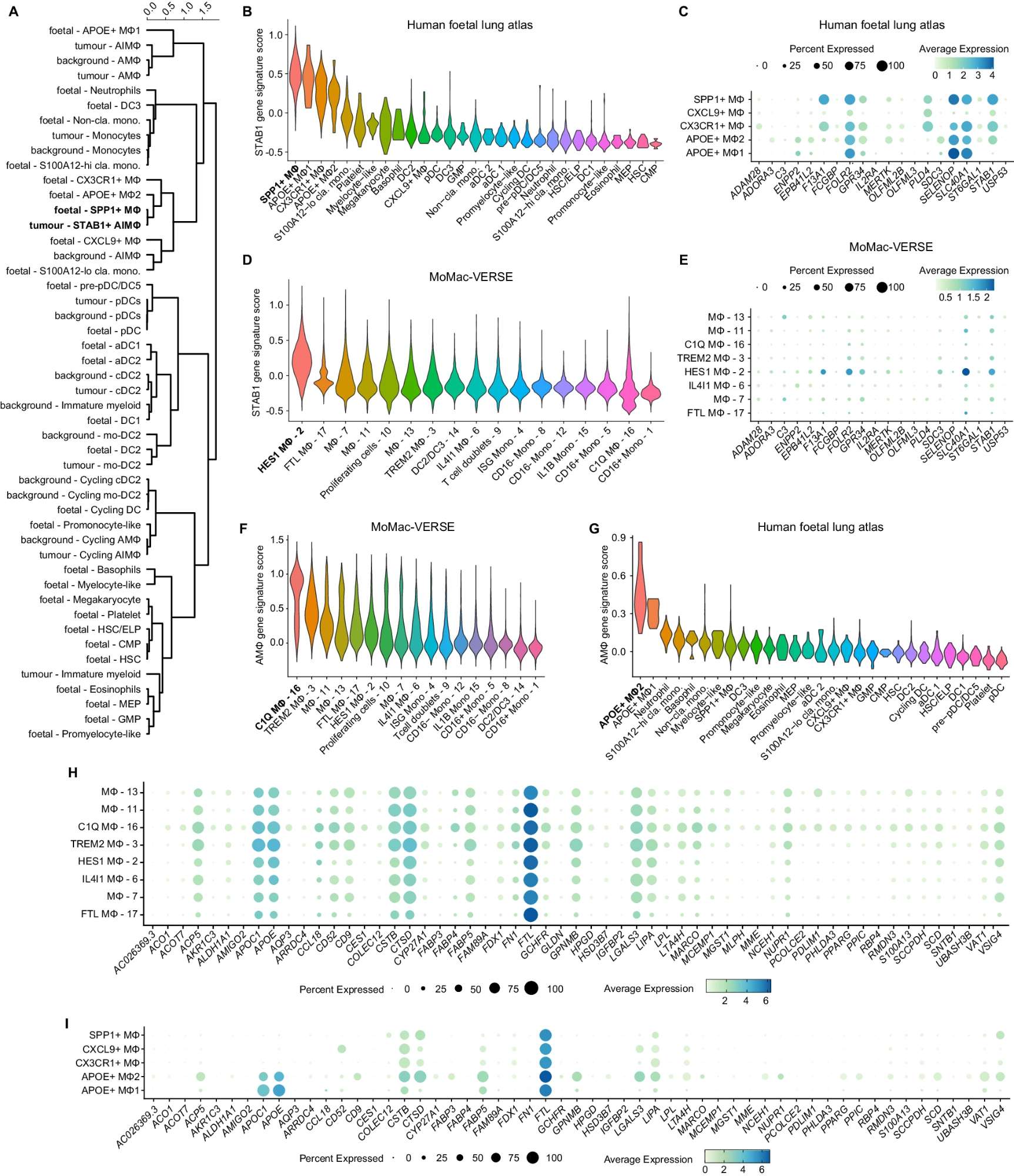
A 层次聚类分析:对在调和后的PC空间(肿瘤髓系 + 背景髓系 + 胎儿肺髓系)的每个细胞计算的相关距离进行层次聚类。
-
B 小提琴图:显示在公开可用的人类胎儿肺图谱中识别的髓系细胞和祖细胞群体中“STAB1基因标志”的表达水平。
-
C 点图:显示选定的胎儿肺巨噬细胞群体中“STAB1基因标志”的每个基因的表达。每个点的大小代表群体中表达该基因的细胞百分比,颜色代表每个群体中每个基因的平均表达水平。
-
D 小提琴图:显示在公开可用的MoMac-VERSE数据集中识别的群体中“STAB1基因标志”的表达水平。
-
E 点图:显示MoMac-VERSE中选定的巨噬细胞群体中“STAB1基因标志”的每个基因的表达。每个点的大小代表群体中表达该基因的细胞百分比,颜色代表每个群体中每个基因的平均表达水平。
-
F 小提琴图:显示在公开可用的“MoMac-VERSE”数据集中识别的髓系细胞和祖细胞群体中“AMɸ基因标志”的表达水平。
-
G 小提琴图:显示在公开可用的人类胎儿肺图谱中识别的髓系细胞和祖细胞群体中“AMɸ基因标志”的表达水平。
-
H 点图:显示“MoMac-VERSE”数据集中识别的选定巨噬细胞群体中“AMɸ基因标志”的每个基因的表达。每个点的大小代表群体中表达该基因的细胞百分比,颜色代表每个群体中每个基因的平均表达水平。
-
I 点图:显示在选定的胎儿肺巨噬细胞群体中“AMɸ基因标志”的每个基因的表达。每个点的大小代表群体中表达该基因的细胞百分比,颜色代表每个群体中每个基因的平均表达水平。
小结
- 主要数据及方法:
| Types | Notes |
|---|---|
| 分析数据 | BioStudies数据库:E-MTAB-13526和E-MTAB-13530,其他的在补充文件里 |
| 分析方法 | 单细胞标准流程(从定量到注释);差异分析;scArches聚类;CellPhoneDB;CopyKAT拷贝数分析;PAGA轨迹分析;cell2location空转标准流程 |
| 实验技术 | 流式;免疫组化和染色;多重免疫荧光 |

魔乐社区(Modelers.cn) 是一个中立、公益的人工智能社区,提供人工智能工具、模型、数据的托管、展示与应用协同服务,为人工智能开发及爱好者搭建开放的学习交流平台。社区通过理事会方式运作,由全产业链共同建设、共同运营、共同享有,推动国产AI生态繁荣发展。
更多推荐
 已为社区贡献16条内容
已为社区贡献16条内容








所有评论(0)